(10分)阅读下表中部分短周期主族元素的相关信息:
请回答:
| 元素代号 | 相关信息 |
| X | X的原子最外层电子数是其内层电子数的三倍 |
| Y | 在第三周期的所用金属离子中,Y的离子半径最小 |
| Z | Z与Y同周期,是所在周期中原子半径最小的元素 |
| T | T的单质能与冷水剧烈反应,生成的强碱电离出两种电子数相等的阴、阳离子 |
(2)单质T与冷水反应的化学方程式为
(3)将Y与Z形成的化合物的水溶液,逐滴加入到T的最高价氧化物对应水化物的溶液中直至过量(边滴加边振荡),写出此过程中发生反应的离子方程式
、 。
(10分)(1)略,离子键、非极性共价键
(2)2Na+2H2O=2NaOH+H2↑
(3) Al3++4OH—= AlO2— +2H2O Al3++3AlO2— +6H2O=4Al(OH)3 ↓ (2分)
考查元素推断及元素周期律
X的电子排布为2、6,即氧元素;
粒子半径决定于电子层数及核电荷数,第三周期中离子的电子层数较小的只有钠离子、镁离子及铝离子,且铝离子核电荷数最大,可知Y为铝元素;
Z是氯元素,第三周期中原子半径最小的元素
T元素为钠元素:短周期中能与冷水反应生成碱的只有钠元素
(1)化合物B为过氧化钠,其电子式为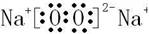
(2)钠与冷水反应:2Na+2H2O=2NaOH+H2↑
(3)AlCl3滴入NaOH溶液中,开始时碱绝对过量,发生的反应为:Al3++4OH—= AlO2— +2H2O;当溶质转变为AlO2—时,继续滴加AlCl3,则发生双水解反应:Al3++3AlO2— +6H2O=4Al(OH)3↓
