某课外小组研究“影响H2O2生成O2快慢的因素”的课题。通过查阅资料,他们提出如下猜想。
【提出猜想】催化剂和反应物浓度都会影响H2O2生成O2的快慢
【实验过程】实验装置图如下:

实验操作:检查装置气密性良好。将分液漏斗中的液体加入锥形瓶中,立即收集一瓶放出的气体。
实验记录:

(1)H2O2溶液和二氧化锰制取氧气的化学方程式为______________。
(2)实验②中加入H2O2的体积为_______mL。
(3)实验③中加入的固体和用量为___________。
【结论】该探究过程得出的结论是___________________。
【反思】H2O2在常温下分解缓慢,加入MnO2后反应明显加快。小红提出,为了更好的证明二氧化锰__________和氯化钠是否对H2O2生成O2快慢有影响,还应该增加一组对比实验。该实验选用的药品和用量为_______。
【实验拓展】小红用收集的气体进行氧气的性质实验。
(4)检验氧气的方法是_________________。
(5)小红发现用该气体进行氧气的性质实验,现象都不明显。造成这种结果的原因是_____________。
【实验过程】
(1)2H2O2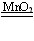 2H2O+O2↑
2H2O+O2↑
(2)100
(3)0.5g二氧化锰
【结论】使用催化剂、增大反应物浓度可以加快H2O2生成O2的速度(或催化剂和反应物浓度都会影响H2O2生成O2的快慢)
【反思】5%H2O2;100mL(不加其他催化剂)
【实验拓展】(4)将带火星的木条插入集气瓶中,木条复燃,证明集气瓶中为氧气。
(5)反应后首先排出的是锥形瓶中的空气,因此立即收集放出的气体中氧气纯度不高,导致铁丝无法在收集的气体中燃烧现象不明显。
