(12分)A、B、X、Y和Z是原子序数依次递增的短周期元素,其中A与Y同主族,X与Z同主族,A与B、A与X均可形成10个电子的化合物:B与Z的最外层电子数之比2:3,常见化合物Y2X2与水反应生成X的单质,其溶液可使酚酞试液变红。
请回答下列问题:
(1)Z的原子结构示意图 ;X原子核外电子排布式为 ;B元素原子的电子排布图 。
(2)A与Y可形成离子晶体的化合物,该化合物的电子式为 ,该化合物与A2X反应的化学方程式 。
(3)化合物Y2X2属于 化合物(“离子”或“共价”),其中含有化学键的类型是 。
(4)B与X可形成三原子化合物,构成该化合物晶体的粒子是 。粒子间的作用力是 。
(5)A与X,A与Z均能形成18个电子的极性分子化合物,此两种化合物的化学式分别是 和 。
(12分)(1)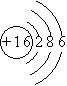 ,
, 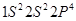 ,
,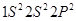
(2)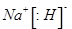 1分,
1分,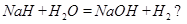 2分
2分
(3)离子化合物 1分,离子键、共价键 1分
(4)分子(或CO2分子) 1分, 分子间作用力(或范德华力)(1分)
(5)H2O2 1分, H2S 1分
由“常见化合物Y2X2与水反应生成X的单质,其溶液可使酚酞试液变红”可知X、Y分别为O、Na元素:2Na2O2+2H2O=4NaOH+O2↑;
由“A与B、A与X均可形成10个电子的化合物”可知:钠的同族元素A为氢;又由于“B与Z的最外层电子数之比2:3”,则B的最外层电子数为4,Z为6,综合可知B为碳元素,Z为硫元素;
(1)硫原子: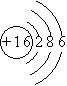 ;氧的核外电子排布式为
;氧的核外电子排布式为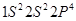 ;B元素原子的电子排布图
;B元素原子的电子排布图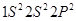
(2)NaH的电子式: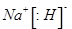 ;它与水发生归中反应:
;它与水发生归中反应: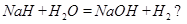
(3)Na2O2由阴阳离子Na+、
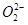 组成,属于离子化合物,包含离子键,
组成,属于离子化合物,包含离子键,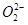 中含有非极性共价键
中含有非极性共价键
(4)CO2为分子晶体,由分子构成,分子间为分子间作用力
(5)18电子微粒分别为H2O2,H2S