问题
实验题
过氧化钠(Na2O2)是一种淡黄色固体,常温下能与水和二氧化碳发生化学反应。某学校两个实验小组的同学为探究其与二氧化碳的反应,用下图所示的装置进行实验。一段时间后,将带余烬的木条插入试管D中,木条复燃。
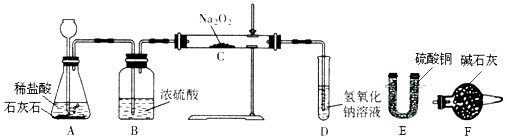
请回答下列问题:
(1)B装置的作用______________。为了检验B装置的作用是否彻底,可在上图______之间(填写装置序号)增加一个________(选填E或F)装置。
(2)第1小组同学认为Na2O2与CO2反应生成了Na2CO3和O2,则该反应的化学方程式为:____________________________。
(3)第2小组同学认为Na2O2与CO2反应除生成Na2CO3和O2外,还有可能生成NaHCO3。你认为呢?简述理由____________________________。
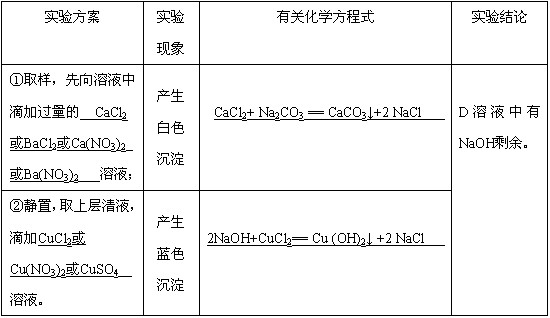
(4)装置D的作用是_______________。有同学设计实验方案,探究反应后试管D的溶液中是否有NaOH剩余,请帮助其完成下列实验报告。

答案
⑴除去水分(防止过氧化钠与水反应);B、C;E
⑵2Na2O2+2CO2==2Na2CO3+O2
⑶不能;根据质量守恒定律,反应物中不含H元素(答出原因才给分)
⑷吸收多余的二氧化碳(防止二氧化碳对检验氧气产生干扰);