以科学原理和实验事实为依据分析问题是学习化学的一种重要方法。
(1)某化学兴趣小组的同学为了鉴别碳酸钠溶液和氢氧化钠溶液,进行了以下实验方案的设计:
①小红:分别取少量待测的溶液少许于两支试管中,分别滴加酚酞试液,观察现象。
②小亮:分别取少量待测的溶液少许于两支试管中,分别滴加澄清的石灰水,观察现象。
经过小组同学认真思考分析,认为小红同学的方法不能达到实验的目的,原因是______; 小组同学按照小亮的实验方案设计进行实验验证,达到了实验目的。写出碳酸钠与氢氧化钙反应的化学方程式:_________。
(2)实验结束后,小组同学将两支试管中的废液倒入同一个干净的烧杯中,看到废液变浑 浊,就对废液进行了过滤,小红和小亮同学对滤液的成分又进行了探究。
【提出问题】滤液中除水外还含有哪些物质?
【作出猜想】小红认为:只含氢氧化钠;
小亮认为:可能含有氢氧化钠和碳酸钠;
你认为还可能是__________(写一种猜想)。
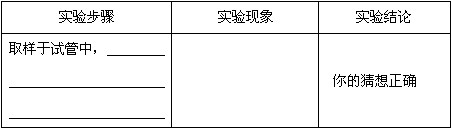
【实验设计】设计一个简单的实验证明你的猜想正确。
【实验分析】小亮同学针对自己的猜想进行了如下实验:

你认为小亮同学对实验结果判断是否正确?请说明理由。_______________________________。
【反思拓展】 ①在分析化学反应后所得物质的成分时,除考虑生成物外还需考虑_________;
②通过以上探究,你认为应怎样处理上述实验后的废液才能倒入下水道?____________。
(1)氢氧化钠和碳酸钠的水溶液都呈碱性,都能使酚酞试液变红 ;Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
(2)【作出猜想】氢氧化钠和氢氧化钙
【实验设计】实验步骤:通入二氧化碳气体(或滴加可 溶性碳酸盐溶液) ;实验现象:试管中出现白色浑浊
【实验分析】不正确,因有氢氧化钠存在,滴入几滴稀盐 酸量太少,稀盐酸会先与氢氧化钠反应,故不会立即出 现气泡,但Na2CO3有可能存在
【反思拓展】①反应物是否有剩余;②在废液中加酸 至溶液的pH =7
