比较和归纳是学习化学的常用方法。某学习小组的同学在下图所列出的实验装置的基础上进行了学习。
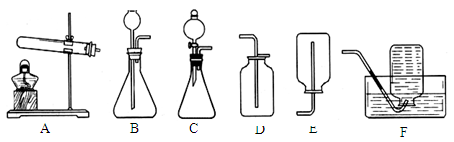
(1)若用B、F组成制取某气体的装置,写出制取此气体的化学方程式为 ,可用B装置还可制取另一气体,写出发生装置中的化学方程式是 。
(2)乙炔(C2H2)是无色、无味、易燃的气体,乙炔的密度比空气略小,微溶于水。乙炔(C2H2)气体和氧气反应能产生高温火焰,工人师傅常用氧炔焰切割或焊接金属。乙炔由碳化钙(块状固体)与水反应生成,同时生成一种白色固体。已知碳化钙与水反应非常剧烈。实验室欲制取并收集纯净的乙炔,要求做到节约、安全、随时发生、随时停止,你选择的装置是 。
(3)如图为某学习小组探究金属化学性质时所做的四个实验,仔细分析后回答下列问题:
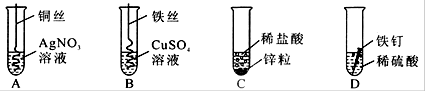
①写出B中反应的化学方程式: 。
②要证明Cu、Fe、Ag的活动性顺序,至少要做的实验是 (填序号)。
(1)2H2O2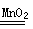 2H2O+O2↑ CaCO3+2HCl=CaCl2+H2O+CO2↑ (2)C F
2H2O+O2↑ CaCO3+2HCl=CaCl2+H2O+CO2↑ (2)C F
(3)①Fe+CuSO4=FeSO4+Cu ②AB
题目分析:(1)B装置属固液在常温反应的发生装置,F是利用排水法收集气体,该组合装置可用于制取和收集氧气或氢气,该发生装置还可用于制取二氧化碳气体;
(2)根据反应物的状态和反应条件选择发生装置,用碳化钙(块状固体)与水反应制取乙炔应选B或C装置,要收集纯净的气体,可采用排水法收集;根据题意,若选用B装置,碳化钙(块状固体)与水接触到后,反应便立即开始,不能人为控制其速率和生成乙炔的量,故要控制其反应速率,可通过控制水的加入量来实现;分液漏斗就可以控制加入液体药品的量和速率;
(3)根据金属活动性顺序的应用,位于前面的金属能把位于后面的金属从化合物的溶液中置换出来,故铁与硫酸铜反应生成的是铜和硫酸亚铁;要证明Cu、Fe、Ag的活动性顺序,至少要做的实验是AB。
