问题
实验题
日常用的干电池构造、组成如图.某校化学活动小组正进行的研究性课题是《回收电池,变废为宝,保护环境——用锌皮制ZnSO4晶体》,请你和他们一道完成下列报告:
研究目的 _________ .
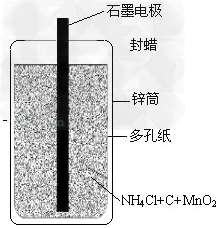
(一)用锌皮制ZnSO4晶体
实验用品: _________ _________ .
实验原理(写出化学方程式): _________ .
实验步骤(简述):
(1) _________ .
(2) _________ .
(3) _________ .
(二)在仅除去了可溶物而回收的干电池的固体物质中除了MnO2外,还含有什么物质,若用这样的MnO2作KClO3热分解制氧气的催化剂会发生什么后果?
答案
研究目的
(1)回收旧电池,了解废旧电池回收利用的方法,
(2)学习用废金属锌制取硫酸锌晶体的方法,练习蒸发结晶和过滤的操作方法;
(一)实验用品:
废旧电池的锌皮、稀硫酸、小烧杯、蒸发皿、玻璃棒、酒精灯、铁架台(带铁夹、铁圈)、漏斗、滤纸等;
实验原理:
Zn+H2SO4═ZnSO4+H2↑;
实验步骤:
(1)拨开废旧电池,将有关表皮、金属锌皮,石墨碳棒、金属铜帽、黑色糊状物等分类放置
(2)将锌皮投入盛有稀硫酸的小烧杯,搅拌,使之完全溶解,
(3)将上述溶液转入蒸发皿中加热蒸发至有大量晶体析出后,停止加热,趁热过滤,滤出的晶体用少量蒸馏水小心冲洗干净,即得硫酸锌晶体;
(二)因为还有一些碳单质留在混合物中,加热条件下氯酸钾分解生成的氧气,碳单质易剧烈燃烧,产生的热量和气体不能及时排出,就会引起爆炸.
