某校学生在探究金属的化学性质时,实验情况如下:
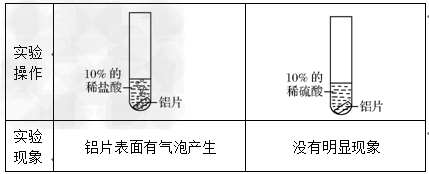
[提出问题]从上述实验现象中,你发现了什么问题? ;
[猜想]针对你发现的问题,分析其原因,大胆提出你的一个猜想: 。
[设计方案]根据你的猜想,任选下列实验用品,进行实验设计。
实验用品:10%的稀硫酸、30%的稀硫酸、相同大小的铝片(若干)、氯化钠试管、试管夹、酒精灯、镊子、药匙、砂纸

(请在考试结束后,到化学实验室实施你的设计方案,验证你的猜想。)
[评价与反思]通过这次探究,你得到的启示或感受是 :
[提出问题]铝片放到稀硫酸中为什么没有现象?
[猜想]可能是铝片表面生成的致密氧化膜阻碍了反应的发生;
或可能与稀硫酸的浓度有关;
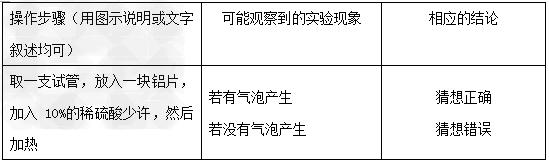
或可能是铝片与稀硫酸反应需要加热;
或Cl-。
[设计方案]方案一

方案二

方案三
方案四
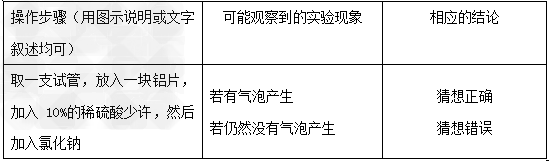
(只要猜想合理,且设计的方案与猜想一致即可)
[评价与反思]:善于发现问题,大胆质疑,勇于探究
