以下是新授课《探究铁的冶炼》的教学过程:
(一)
【老师提问】
(1)炼铁就是把Fe2O3等铁的氧化物转变为Fe的过程,即使Fe2O3等金属氧化物失去 _________ 元素的过程.
(2)Mg、C、CO等都能与O2反应,写出与O2反应的一种气体单质 _________ .
【老师分析】
(1)这些物质都能与O2反应,也就是都能和氧元素结合,或者说是能夺取氧元素,分别生成MgO、CO2、CO2.
【提出问题】
一氧化碳能夺取Fe2O3中的氧元素吗?
【实验验证】
按下图进行实验,证明CO确实能和Fe2O3发生化学反应.学生完成学案:

(1)A、B处发生的现象分别是 A _________ 、B _________ ;
(2)如何简单地检验生成了铁 _________ .
(3)C处尾气如何处理? _________ .
(4)若进行上述反应时,用的是生锈的铁片样品10克,经测定B中石灰水溶液的质量增3.3g,通过计算求出生锈的铁片样品中Fe2O3的质量分数.(请写出计算过程)
(二)
【反思拓展】
复习课上,老师对炼铁原理进行反思,又设计了两个问题:
(1)下图中B是红色固体单质.C为红色固体,具有疏松多孔的结构.A是黑色固体.

①A物质的化学式为 _________ .
②实现④过程的化学方程式是 _________ .
③实现③过程需要的条件是 _________ .
④实现②过程除了可通入H2、CO外,还可加入一种固体单质,该单质是 _________ .
(三)
(2)按下列实验过程完成表格:

(1)氧
(2)氢气
(1)红色固体变为黑色;澄清的石灰水变浑浊
(2)用磁铁吸引.
(3)点燃或收集.
(4)设10g样品中氧化铁的质量为x
3CO+Fe2O3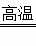 2Fe+3CO2
2Fe+3CO2
160 132
x 3.3g

x=4g
故样品中氧化铁的质量分数为: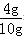 ×100%=40%
×100%=40%
(五)反思拓展
(1)①Fe3O4.
②Fe+CuSO4=FeSO4+Cu
③潮湿的空气中
④碳
(2)①红亮的铜丝变为黑色;2Cu+O2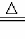 2CuO
2CuO
②黑色的氧化铜变为红色;CuO+CO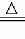 Cu+CO2
Cu+CO2
