某品牌纯碱中含有少量氯化钠。某化学探究小组为了测定该纯碱的纯度(即碳酸钠的质量分数),组内一同学设计了如下实验:
【设计实验方案】实验装置(如图2所示,固定装置略去):
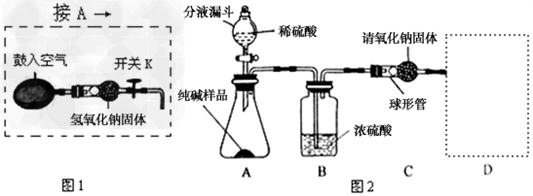
需要测定的实验数据:纯碱样品的质量;实验前后C装置(包含氢氧化钠固体)的质量。
(1)A装置中反应化学方程式是 。纯碱样品中的碳酸钠完全反应,其操作是 。
(2)B装置的作用是 ;C 装置的化学方程式是是 ;
(3)补充D装置  (简要叙述或画出装置示意图)。
(简要叙述或画出装置示意图)。
【交流与表达】
(4) 有同学认为图2 所示实验装置会造成测得纯碱的纯度偏低,原因是 。
(5) 为了克服图2 装置的不足,有同学提出,还应增加图1 装置与A 装置连接(A 装置中原双孔橡胶塞换成三孔橡胶塞),在反应前、后用图1 装置分两次缓缓鼓入空气。
①反应前,断开B 、C 装置之间的连接,用图1 装置鼓入空气的作用是 。 ②反应后,用图1 装置鼓入空气的作用是 。 ③在A 装置中的反应发生时,开关K 处于关闭状态,其原因是 。
【数据处理】
(6)称得纯碱样品的质量为10.8g,实验前、后C装置的总质量分别为75.2g和79.6g,纯碱的纯度为 %(计算结果保留小数点后1位)。
【反思与评价】
(7)能否用稀盐酸代替稀硫酸?同学们经过讨论认为不能,理由是 。
(8)改进后的实验装置能减少测定的误差,原因是①反应生成的CO2尽可能被装置C 吸收;② 。
(1) Na2CO3+H2SO4=Na2SO4+H2O+CO2↑ ; 逐滴滴入稀硫酸至不再产生气泡为止 。
(2) 除去水蒸气 ; 2NaOH + CO2 = Na2CO3+ H2O
(3)装NaOH固体的球形管 
(4) A 、B装置中残留的CO2 气体未被装置C中的NaOH 吸收
(5) ① 用不含二氧化碳的空气排出A 、B装置中原有的空气 。
② 用不含二氧化碳的空气排出残留在A 、B装置中的 CO2 。
③ 避免图1装置吸收反应产生的部分二氧化碳气体 。
(6) 98.1 %
(7) 稀盐酸挥发出氯化氢气体被装置C吸收,影响实验测定 。
(8) 避免A 、B装置中原有空气所含二氧化碳气体对实验的干扰 。
