(本小题满分16分)
Ⅰ.汽车尾气(含有烃类、CO、SO2与NO等物质)是城市空气的污染源。治理的方法之一是在汽车的排气管上装一个“催化转换器”(用铂、钯合金作催化剂)。它的特点是使CO与NO反应,生成可参与大气生态环境循环的无毒气体,并促使烃类充分燃烧及SO2的转化。
(1)写出一氧化碳与一氧化氮反应的化学方程式
(2)“催化转换器”的缺点是在一定程度上提高空气的酸度,其原因是
(3)控制城市空气污染源的方法可以有 (多选扣分)
a.开发氢能源 b.使用电动车 c.植树造林 d.戴上呼吸面具
Ⅱ.A、B、C、D、E五种短周期元素,原子序数E>D>A>B>C,且A、B、D、E同周期,A、C同主族,A的原子结构示意图如图,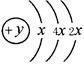 B的最外层电子数比K层电子多1,
B的最外层电子数比K层电子多1,
D元素的主族序数是周期序数的2倍,E的单质是黄绿色气体;据此填空:
(1) 指出元素A在周期表中的位置 ,其气态氢化物的化学式为 。
(2) D和E两种元素相比较,非金属性较强的是(填元素符号) ,
可以验证该结论的是(填写字母序号) ;
A.比较这两种元素的常见单质的熔沸点 B.比较这两种元素的气态氢化物的熔沸点
C.比较这两种元素的气态氢化物的稳定性 D.比较这两种元素置换能力的强弱
(3)C、D、E三种元素最高价氧化物的水化物的酸性由强到弱的顺序: 。(填写化学式)
Ⅰ.(1)2CO + 2NO 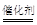 2CO2 + N2,(2)SO2转化成SO3,产生硫酸酸雾。
2CO2 + N2,(2)SO2转化成SO3,产生硫酸酸雾。
(3)a、b。
Ⅱ.(1)第三周期IVA族,SiH4 (2) Cl CD
(3)HClO4>H2SO4>H2CO3
Ⅰ.(1)参与大气生态环境循环的无毒气体应该是CO2和氮气,所以方程式为2CO + 2NO 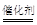 2CO2 + N2。
2CO2 + N2。
(2)“催化转换器”能促使SO2的转化,而SO2是转化为SO3的,而SO3易形成酸雨,从而产生硫酸酸雾。
(3)植树造林可以改善大气环境,但不能控制城市空气污染源。戴上呼吸面具是不现实的。
Ⅱ.第一层只能容纳2个电子,所以x等于2,故该元素的原子序数是14,即A是硅,原子序数E>D>A>B>C,A、C同主族,则C是碳。短周期元素中最外层电子数比K层电子多1的元素可以是B或者是Al,由于B的原子序数大于碳的,所以B只能是铝。A、B、D、E同周期,属于第三周期,D元素的主族序数是周期序数的2倍,所以D是硫元素。E的单质是黄绿色气体,则E是氯元素。
