某化学兴趣小组的同学对 “硫酸、硝酸钡、氢氧化钠、碳酸钠”四种物质之间的反应进行了定性和定量的研究。根据复分解反应发生的条件,初步判断上述四种溶液两两之间能发生_____________个反应;其中有气体、沉淀生成的化学方程式为:(请各写出一个)
(1)_______________;
(2)_______________ 。
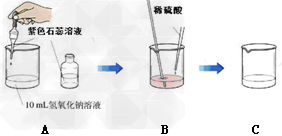
【实验一】证明氢氧化钠溶液和稀硫酸混合后确实发生了化学反应王同学按下列方法进行了实验: 请回答:在A的实验中,滴入紫色石蕊溶液的目的是___________; B装置中发生的化学反应方程式为_____________;
【实验二】定量分析稀硫酸与两种混合物反应后溶液的成分刘同学称取38.2g氢氧化钠和碳酸钠的混合溶液于烧杯中,向其中逐滴滴加质量分数为15.3%的稀硫酸,同时记录实验数据,测得加入稀硫酸的质量与生成气体的质量关系如图所示。
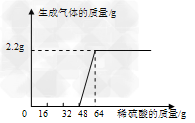
①当加入16g稀硫酸时,溶液中的溶质为_____________(写化学式)
②求混合物与稀硫酸恰好完全反应时所得溶液的溶质质量分数。_____________(请写出计算过程,结果保留到0.1%)
【实验三】实验分析四种化合物溶液混合后的成分洪同学按以下流程进行了实验:
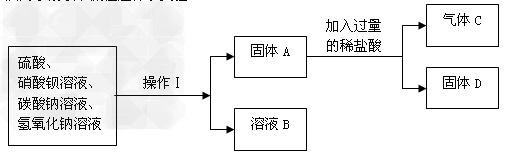
操作Ⅰ的名称是_____________,固体D的化学式是___________; 如溶液B中滴入酚酞,呈无色,则B中一定没有____________离子;一定含有____________离子。
4 ;
(1)Na2 CO3+ H2SO4 =Na2SO4+H2O+CO2↑ ,
CO3+ H2SO4 =Na2SO4+H2O+CO2↑ ,
(2) H2SO4+Ba(NO3)2 =BaSO4↓+ 2HNO3 或Ba(NO3)2+Na2CO3=BaCO3 ↓+ 2NaNO3
【实验一】证明氢氧化钠溶液和稀硫酸是否发生反应 ;
2NaOH + H2SO4 = Na2SO4 + 2H2O
【实验二】①NaOH 、Na2CO3、Na2SO4
②解:当混合物与稀硫酸恰好完全反应时所用稀硫酸中溶质的质量为
64g ×15.3% ≈ 9.8g
当混合物与稀硫酸恰好完全反应时所得溶液中的溶质质量为:
9.8g ×(142 /98 )=14.2g
当混合物与稀硫酸恰好完全反应时所得溶液中的溶质质量分数为:

【实验三】过滤;BaSO4; OH-;Na+、NO3-。
