化学兴趣小组的同学为了测定某赤铁矿石中氧化铁的质量分数。
Ⅰ.甲同学取一定质量的赤铁矿粉与过量的木炭粉混合后,用下图所示装置以合理的操作步骤测定(假设杂质始终不发生变化)。
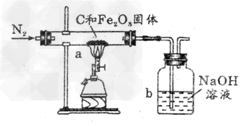
① 实验中持续通入干燥的氮气。加热前缓缓通入一段时间,其作用是_________________
② 反应结束后,甲同学熄灭了喷灯的火焰后,马上停止通入N2,他的操作对吗?_________ 说明理由_______________
③如果氢氧化钠溶液是足量的,对二氧化碳的吸收是完全的,那么甲同学用氢氧化钠溶液的增重测定出氧化铁的质量分数将___________(选填“偏大”、“偏小”或“准确”),原因是____________,若有误差,则减小误差的改进措施是__________________。
Ⅱ.乙同学取矿石样品10g,加入足量稀盐酸,完全反应后,共用去稀盐酸112.5g,过滤得到滤渣2.5g (假设杂质既不溶于水也不与酸发生反应)。请你和乙同学—起计算赤铁矿石中氧化铁的质量分数和反应后溶液中氯化铁的质量分数。(计算过程中保留二位小数,最后精确到0.1%)
①将装置内的空气排尽
②不对;b 中的NaOH 溶液会倒吸入a 中造成硬质玻璃管破裂
③偏小; 氢氧化钠增重的质量因一氧化碳的生成和气体带走的水蒸气而偏小;在ab 之间再连一个盛有氧化铜的两头通的玻璃管和a 装置同时加热,在b 后连一个干燥装置和b 一起称增重。
Ⅱ. 铁矿石的质量分数=(10g-2.5g)/10g ×100%=75%
设和7.5g Fe2O3反应生成FeCl3质量为x 。
Fe2O3 + 6HCl === 2FeCl3 + 3H2O
160 325
7.5g x
160:325=7.5g:X , X=15.23g
溶液中FeCl3的质量分数=15.23g/(7.5g+112.5g) ×100% =12.7%
