(第(1)小题每空1分,其余每空2分,共12分)
A、B、C、D四种短周期元素,原子序数依次增大,A、C同主族,C、D同周期,B原子最外层电子数是最内层电子数的3倍。A、B可形成A2B和A2B2两种液态化合物,B、C也可形成C2B和C2B2两种固态化合物。C+具有与氖原子相同核外电子排布。D原子最外层电子数比B原子最外层电子数多一个电子,根据以上条件,判断:
(1)四种元素分别是(写元素符号) A B C D
(2)用电子式写出A2B化合物的形成过程___; 用电子式写出C2B化合物的形成过程___;
(3)A2B2中加少量MnO2反应的化学方程式________;C2B2与CO2反应的化学方程_____。
(1)H O Na Cl (写名称不得分)
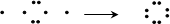 (2) H + O + H H O H ;
(2) H + O + H H O H ;


 Na + O + Na
Na + O + Na 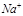 [ O ]
[ O ]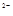
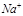 (未标电子转移方向可不扣分)
(未标电子转移方向可不扣分)
MnO2 |
“B原子最外层电子数是最内层电子数的3倍”,则B的核外电子排布为2 6或2 8 6
再结合“A、B可形成A2B和A2B2两种液态化合物,B、C也可形成C2B和C2B2两种固态化合物,C+具有与氖原子相同核外电子排布”,得:A是氢元素、B是氧元素、C是钠元素;D的核外电子排布为2 8 7,所以D为氯元素;
