问题
填空题
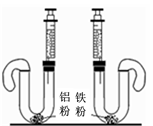
如图所示,两只U型管中分别加入纯净、等物质的量的铝粉 和铁粉,同时将两端注射器内的液体(等质量、浓度为20%的 稀硫酸)快速注入U型管中。
Ⅰ.写出铁粉与稀硫酸发生反应的化学方程式 (16) 。
Ⅱ.反应结束并冷却至室温,发现左端气球膨胀程度明显大于右端,若仅有一只U型管内的硫酸有剩余, 则是 (17) (填“左”或“右”)端的U型管。
Ⅲ.若将铝粉和稀硫酸换成其他两种化合物(或其溶液),也能观察到气球明显膨胀,这两种物质可能是(写化学式) (18) 。
答案
(16) Fe+ H2SO4→H2↑+ FeSO4;(17)右;(18)Na2CO3 HCl
题目分析:Ⅰ.铁粉与稀硫酸发生反应的化学方程式为Fe+ H2SO4→H2↑+ FeSO4; Ⅱ.反应结束并冷却至室温,发现左端气球膨胀程度明显大于右端,说明左端生成的氢气多,消耗的盐酸多,故若仅有一只U型管内的硫酸有剩余,则是右端的U型管。Ⅲ.若将铝粉和稀硫酸换成其他两种化合物(或其溶液),也能观察到气球明显膨胀,根据反应原理是物质反应生成气体,故这两种物质可能是Na2CO3和HCl
