某研究小组对用H2O2分解生成H2O和O2的实验条件进行探究.他们进行了以下实验:
①往盛有5mL 5% H2O2溶液的试管中,伸入带火星的木条,木条不复燃.
②往盛有5mL w% H2O2溶液的试管中,加入a g MnO2,伸入带火星的木条,木条复燃.
③往盛有5mL w% H2O2溶液的试管中,加入a g Fe2O3,伸入带火星的木条,木条复燃.
④经检验,②、③中反应后试管中仍分别含有a g MnO2和a g Fe2O3.
问题:
(1)MnO2、Fe2O3在上述反应中的作用是 _________ .
(2)实验 ②、③中H2O2的浓度(w%)以 ____ ___ 为宜,你的理由是 _ _ _______ .
(3)写出实验②化学反应的方程式 ___ ______ .研究小组还对溶液浓度、催化剂的种类等实验条件进行了探究.
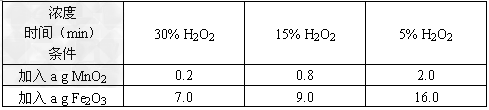
下表选取了部分实验数据:用足量等体积H2O2溶液制取相同体积O2所需的时间.
问题:
(4)从上表中能得出哪些结论?
① ______ ___ _;②____ _____;
(5)再写出一个用MnO2作催化剂的化学反应方程式_____ ____.
(1)催化作用
(2)5%; 在体积和过氧化氢溶液的溶质的质量分数都相同的条件下实验,才能比较出不加催化剂和加入二氧化锰或氧化铁后的催化作用.
(3)2H2O2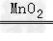 2H2O+O2↑
2H2O+O2↑
(4)
①相同条件下,MnO2的催化效果比Fe2O3好
②在其他条件相同的情况下,H2O2浓度越大,产生氧气的速度越快.
(5)2KClO3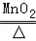 2KCl+3O2↑
2KCl+3O2↑