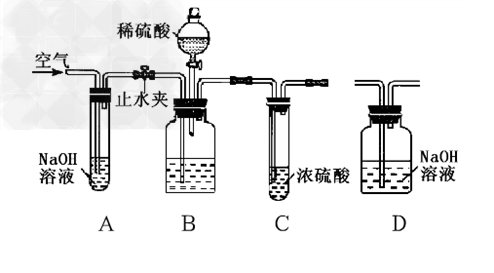
工业纯碱中常含有少量的NaCl 杂质。下图是测定纯碱样品中Na2CO3质量分数的实验装 置,反应的化学方程式为:Na2CO3 + H2SO4==Na2SO4 + H2O + CO2↑。(装置气密性良好,纯碱样品质量为11.0 g,装置D反应前的质量为172.2 g)。
操作步骤为: ①将样品装入B装置广口瓶中→打开止水夹,缓缓鼓入空气数分钟;
②连接装置D→关闭止水夹,向盛有样品的广口瓶中滴加稀硫酸至不再产生气泡;
③打开止水夹,再次缓缓鼓入空气数分钟;
④称量反应后装置D的质量为176.6 g。(假设每套装置均反应完全)。
(1)在实验过程中装置D吸收二氧化碳 g,计算纯碱样品中Na2CO3。
(2)如果去掉C装置,则测定结果 (填序号)。
①偏大 ②偏小 ③不变
(1)4.4
解:设11.0g纯碱样品中Na2CO3的质量为X
Na2CO3 + H2SO4= Na2SO4 + H2O + CO2↑
106 44
X 4.4g
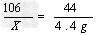
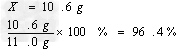
(2 ) ①
