同学们在学习碱的化学性质时,进行了如图所示的实验.
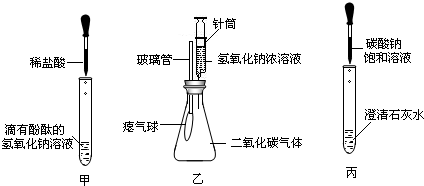
(1)写出甲实验中盐酸和氢氧化钠反应的化学方程式______.
(2)乙实验中滴加氢氧化钠溶液后,可观察到的现象是______.
(3)丙实验中观察到试管内有白色沉淀产生.
(4)实验结束后,同学们将甲、乙、丙三个实验的废液倒入同一个干净的废液缸中,最终看到废液浑浊并呈红色,产生疑问.
【提出问题】:
废液中含有哪些物质?
【交流讨论】:
①一定含有的物质:碳酸钙、指示剂、水和______(写物质名称).
②还含有能使废液呈碱性的物质.能使废液呈碱性的物质是什么?同学们有如下猜想.
小云认为:只有碳酸钠
小红认为:只有氢氧化钙
小林认为:是氢氧化钠和碳酸钠你认为还可能是______.(写一种猜想)
【实验设计】:
小方想用氯化钙溶液来验证小云、小红、小林的猜想.查阅资料获悉氯化钙溶液呈中性,并设计如下实验.请你将小方的实验设计补充完整.小云认为:只有碳酸钠
| 实验内容 | 预计现象 | 预计结论 |
| 取少量废液缸中上层清液于试管中,加入过量氯化钙溶液,静置. | ①有白色沉淀,溶液呈红色. | ______的猜想正确. |
| ②______ | ______的猜想正确. | |
| ③______ | ______的猜想正确. |
在分析化学反应后所得物质的成分时,除了考虑生成物外还需考虑______.
(1)反应的反应物为盐酸和氢氧化钠,生成物为氯化钠和水,直接已经平了;
(2)氢氧化钠溶液与二氧化碳反应使瓶内压强减小,在外界大气压的作用下空气进入气球;
(4)根据实验探究的步骤可推出:提出问题和交流讨论.①盐酸与氢氧化钠反应一定生成氯化钠,并且氯化钠显中性不与其它物质反应,所以一定含有氯化钠;②由于丙实验中是碳酸钠与氢氧化钙反应生成碳酸钙和氢氧化钠,所以可能含有氢氧化钠;加入过量氯化钙,有沉淀说明含有碳酸钠,加过量的氯化钙已经把碳酸钠除净,溶液呈红色说明含有碱,所以小林猜想正确;如果有白色沉淀,溶液由红色变为无色,说明只有碳酸钠没有碱,故小云猜想正确;没有白色沉淀,溶液呈红色,说明没有碳酸钠,有碱,故小红猜想正确;在分析化学反应后所得物质的成分时,除了考虑生成物外还需考虑反应物是否有剩余.
故答案为:(1)NaOH+HCl═NaCl+H2O
(2)气球胀大
(4)【交流讨论】①氯化钠②氢氧化钠(合理答案均可)
【实验设计】
①小林
②有白色沉淀,溶液由红色变为无色;小云
③没有白色沉淀,溶液呈红色;小红
【反思拓展】反应物是否有剩余(合理答案均可)

 Ⅰ度松动,叩痛(+),患者不能指明患牙位置,颊侧近中窄而深牙周袋10mm,X线片见左侧上后第一磨牙近中根管中下段均匀增宽,远中根牙槽骨未见吸收
Ⅰ度松动,叩痛(+),患者不能指明患牙位置,颊侧近中窄而深牙周袋10mm,X线片见左侧上后第一磨牙近中根管中下段均匀增宽,远中根牙槽骨未见吸收