(12分)下表是元素周期表的一部分,请回答有关问题:
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | ||||||
| 2 | ① | ② | ③ | |||||||||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||||||||
| 4 | ⑨ | ⑩ |
小题2:表中能形成两性氢氧化物的元素是 (用元素符号表示),写出该元素的单质与⑨最高价氧化物的水化物反应的化学方程式 。
小题3:①、②、⑥、⑦四种元素的最高价氧化物的水化物中酸性最强的是 (填化学式)。
小题4:③元素与⑩元素两者核电荷数之差是 。
小题5:设计实验方案:比较⑦与⑩单质氧化性的强弱,请将方案填入下表。
| 实验步骤 | 实验现象与结论 |
小题1: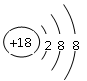
小题2:Al(2分), 2Al+ 2KOH+2H2O ="==" 2KAlO2+3H2↑ (2分)
小题3:HClO4(2分)
小题4:26 (2分)
小题5:(4分)
| 实验步骤(2分) | 实验现象与结论(2分) |
| 将少量氯水加入盛有溴化钠溶液的试管中,振荡后,加入少量四氯化碳,振荡 | 若加入氯水后溶液呈黄色,加入少量四氯化碳后,四氯化碳层呈棕色,证明单质氯比单质溴氧化性强。 |
考查元素周期表的结构和元素周期律的应用。根据元素在周期表中的位置可判断①~⑩分别为C、N、F、Mg、Al、S、Cl、Ar、K、Br。
小题1:最不活泼的是稀有气体元素Ar,其原子结构示意图为 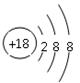
小题2:氢氧化铝是两性氢氧化物,单质铝可溶解在强碱氢氧化钾中,反应式为2Al+ 2KOH+2H2O ="==" 2KAlO2+3H2↑。
小题3:非金属性越强,最高价氧化物的水化物的酸性越强,在已知元素中Cl的非金属性最强,最高价含氧酸的酸性最强,化学式为HClO4。
小题4:F和Br的原子序数分别是8和35,核电荷数之差是26.
小题5:比较非金属性强弱时可以元素周期律,也可以利于最高价氧化物的水化物的酸性强弱,或者是非金属单质和氢气化合的难易程度以及相应氢化物的稳定性,或者是非金属之间的相互置换能力等。因此可以通过氯气和溴化钠的置换反应进行比较。
