问题
填空题
(1)已知锌与稀硫酸反应为放热反应,某学生为了探究其反应过程中的速率变化,用排水集气法收集反应放出的氢气,实验记录如下:
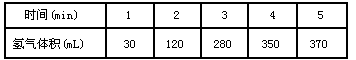
①反应速率最大的(即0 min~1 min、1 min~2min、2 min~3min、 3 min~4 min、4 min~5 min)时间段为_____________,原因是______________。
②反应速率最小的时间段为______________,原因是_________________。
(2)另一学生也做同样的实验,由于反应太快,测量氢气的体积时不好控制,他就事先在硫酸溶液中分别加入等体积的下列哪些溶液以减慢反应速率。
A.蒸馏水 B.CuCl2溶液 C.NaCl溶液
你认为他的做法可行的是____________(填相应编号);做法不可行的理由是__________________。
答案
(1)①2min~3 min ;因该反应是放热反应,此时温度高
②4 min~5min ;此时H+浓度小
(2)AC ;置换出Cu,形成Cu-Zn原电池反应,使反应加快
