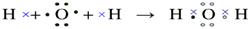(9分)现有10种元素的性质、数据如下表所列,它们均为短周期元素。回答下列问题:
| A | B | C | D | E | F | G | H | I | J | |
| 原子半径(10-9m) | 0.074 | 0.160 | 0.152 | 0.110 | 0.099 | 0.186 | 0.075 | 0.082 | 0.102 | 0.037 |
| 最高或最低 化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | +6[ | +1 | |
| -2 | -3 | -1 | -3 | -2 |
(2)在以上元素形成的最高价氧化物的水化物中,酸性最强的化合物的分子式是 。
(3)化合物F2A2的电子式是: ,构成该物质的化学键类型为________________(填“离子键、极性键或非极性键”)
当F2A2与J2A的反应中有3.01×1023个电子转移时,参加反应的F2A2的质量是 g。
(4)用电子式表示J2A的形成过程: ;
(1) B; 第三周期第IIA族; (2)HClO4;
(3) 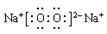 离子键、非极性键;39g
离子键、非极性键;39g
(4)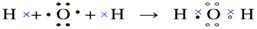
(第(4)题2分,如果电子分别用点和叉表示了,则前后点叉必须对应,否则没分)
第(3)题第二个空“离子键、非极性键”2分,填对一个给一分,其余每题每空1分
考查元素周期律的应用。同周期自左向右原子半径逐渐减小,最高正价逐渐增大。同主族自上而下原子半径逐渐增大。从非金属元素开始出现负价。元素的最高价就是主族元素的价电子。所以根据元素的主要化合价和主要半径可知,A~J分别是O、Mg、Li、P、Cl、Na、N、B、S、H。化合物F2A2的是过氧化钠,含有离子键和非极性键,电子式为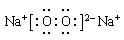 。J2A是水,和过氧化钠反应的方程式为2Na2O2+2H2O=4NaOH+O2↑,在反应中过氧化钠既是氧化剂也是还原剂,每消耗2mol过氧化钠,反应中就转移2mol电子。所以有3.01×1023个电子转移时,参加反应的F2A2的质量是0.5mol×78g/mol=39g。水是由极性键构成的共价化合物,其形成过程为
。J2A是水,和过氧化钠反应的方程式为2Na2O2+2H2O=4NaOH+O2↑,在反应中过氧化钠既是氧化剂也是还原剂,每消耗2mol过氧化钠,反应中就转移2mol电子。所以有3.01×1023个电子转移时,参加反应的F2A2的质量是0.5mol×78g/mol=39g。水是由极性键构成的共价化合物,其形成过程为