(10分)下图为周期表中的一部分。已知A、B、C、D均为短周期元素,A与D原子序数之和为C原子序数的1 .5倍。
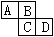
(1)B元素符号是: _______、D在元素周期表中第_______族。
(2)四种元素中原子半径最大的是(填元素符号)_______,B、C、D三种离子中半径最大的是(填离子符号)_______。
(3)B比C的氢化物的沸点高是因为_____ __;A、D两元素的气态氢化物相互反应的生成物的电子式: ,其中存在_______键、_______(填“极性”或“非极性”)共价键。
(4)写一个离子方程式证明C和D的非金属性相对强弱: 。
(1)O、第VIIA族。(2)S,S2-。(3)水分子间有氢键;
: 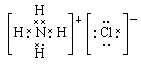 ;离子、极性(4) S2- +Cl2 ===S↓+2Cl-
;离子、极性(4) S2- +Cl2 ===S↓+2Cl-
若设A的原子序数是x,则B是x+1,C是x+9,D是x+10。A与D原子序数之和为C原子序数的1 .5倍,即x+x+10=1.5×(x+9),解得x=7。所以A是N,B是O,C是S,D是Cl。同周期自左向右原子半径逐渐减小,同主族自上而下原子半径逐渐增大,所以原子半径最大的是硫。对于核外电子排布相同的微粒,其微粒半径随原子序数的增大而减小,所以B、C、D三种离子中半径最大的是S2-。水中含有氢键,所以水的沸点硫化氢的。氨气和氯化氢反应生成氯化铵,属于离子化合物,含有离子键和极性键。可以根据非金属性较强的能把较弱的从其盐溶液中置换出来,比较其非金属性强弱。
