问题
填空题
(11分)某化学兴趣小组同学在实验室里收集了一些溶质为FeSO4和CuSO4的废液,想从中回收金属铜和硫酸亚铁溶液,设计了如下方案:
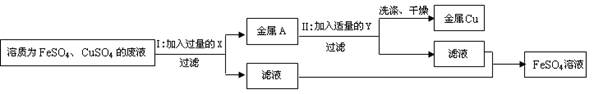
(1)步骤Ⅰ中有关反应的化学方程式是 。
(2)步骤Ⅱ中所加试剂Y的名称为 。
(3)加入过量X的目的是 。
(4)步骤Ⅰ和Ⅱ中都有过滤操作,所需要的玻璃仪器有 、 和 。
(5)步骤Ⅱ中经过过滤、洗涤、干燥可以得到纯净的金属铜,洗涤时检验金属铜是否已洗净的方法是 。
答案
(1)Fe+CuSO4===Cu+FeSO4(2分)(2)稀硫酸(1分)
(3)使CuSO4完全转化为FeSO4(2分)
(4)漏斗 (1分) 烧杯 (1分) 玻璃棒(1分)(不分先后顺序)
(5)取最后洗涤液少量,滴加适量氯化钡溶液(或硝酸钡溶液、氢氧化钡溶液),若无沉淀产生,则证明金属铜已洗净(3分)(不写现象扣1分)
解答类似的题目要从实验要达到的目的来入手思考,由于目的是获得铜单质和硫酸亚铁,所以需要将铜离子转化为铜单质,而溶液中需要的是硫酸亚铁而不能引入新的杂质,所以加入的能够将铜离子转化为铜单质的只能是单质铁.以及实验仪器,和实验基本操作进行解答
