碱式碳酸铜[化学式Cu2(OH)2CO3,相对分子质量为222]加热完全分解后生成的黑色固体是什么?甲、乙、丙、丁四位同学对此进行探究.请你与他们一起,踏上探究之路.
(1)他们称取了2.5g碱式碳酸铜在试管中加热使之完全分解,冷却至室温后,称量黑色固体产物质量为1.8g.结合碱式碳酸铜的化学式,他们对黑色固体产物做出以下猜想:
a、可能是氧化铜; b、可能是炭粉; c、可能是氧化铜和炭粉的混合物.他们做出以上猜想的依据是______.
(2)甲同学从资料中得知:碳、氢气、一氧化碳在加热或高温条件下都能夺取一些金属氧化物中的氧,使其变为金属单质.他认为猜想C可以排除,理由是______.
(3)乙同学通过对得到的实验数据进行计算分析.排出了猜想b,他的理由是______.
(4)黑色固体究竟是什么?
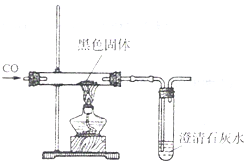
丙同学设计的实验方案:向盛有少量该黑色固体的试管中加入足量的稀硫酸,充分振荡后,静置观察.黑色固体消失,溶液变蓝.丁同学设计的实验方案(如右图所示):在盛有少量该黑色固体的玻璃管中,通入一氧化碳后加热.黑色固体逐渐变成光亮的红色,澄清石灰水变浑浊.他们根据实验现象都得出结论:黑色固体是氧化铜.丙、丁两同学的实验方案,______
(填丙同学或丁同学)较好,谈谈你的看法:______.(简答一条)
(5)科学探究的方法和途径有多种,只要善于思考,就会有惊喜的发现.根据实验数据进行计算分析,也可以得出结论:黑色固体是氧化铜.理由是______.
(1)根据质量守恒定律可知,反应前后元素的种类不变;碱式碳酸铜[Cu2(OH)2CO3]的产物是有Cu、O、H、C中的一种或多种元素组合而成;结合题目信息(黑色粉末)可知,氧化铜和碳都是黑色固体;所以黑色物质可以是题目所说的三种情况
(2)氧化铜和碳在高温条件下发生反应生成铜和二氧化碳,所以在高温条件下,氧化铜和碳不会同时存在
(3)2.5g碱式碳酸铜中碳元素的质量为:2.5g×
≈0.14g<1.8g 碱式碳酸铜中碳元素质量小于黑色固体的质量,所以不可能是碳12 222
(4)丁同学方案一氧化碳还原氧化铜需加热,一氧化碳有毒,逸散到空气中会污染空气等.故丙同学方案好
(5)设2.5g碱式碳酸铜能得到氧化铜的质量为x,根据质量守恒
Cu2(OH)2CO3~2CuO
222 2×80
2.5g x
=222 2.5g
x≈1.8g 与生成黑色固体的质量相等,则黑色固体产物为氧化铜.2×80 x
2.5g碱式碳酸铜可转化为CuO的质量为:2.5g×
÷2×64 222
≈1.8g与生成黑色固体质量相等,故黑色固体产物为氧化铜64 80
故答案为:(1)①化学反应前后元素种类不变且氧化铜和炭粉都是黑色固体
(2)①炭粉与氧化铜在加热或高温的条件下能发生反应
(3)①2.5g×
≈0.14g<1.8g 碱式碳酸铜中碳元素质量小于黑色固体的质量12 222
(4)①丙同学
②丁同学方案需加热或操作复杂或易污染空气等(答对一点给分)
(5)①设2.5g碱式碳酸铜能得到氧化铜的质量为x,根据质量守恒
Cu2(OH)2CO3~2CuO
=222 2.5g
x≈1.8g与生成黑色固体的质量相等,则黑色固体产物为氧化铜.2×80 x
或2.5g碱式碳酸铜可转化为CuO的质量为:2.5g×
÷2×64 222
≈1.8g与生成黑色固体质量相等,则黑色固体产物为氧化铜.64 80
