W、X、Y、Z为短周期内除稀有气体外的4种元素,它们的原子序数依次增大,其中只有Y为金属元素;Z元素的最高正化合价为+6。Y和W的最外层电子数相等。Y、Z两元素原子的质子数之和为W、X两元素质子数之和的3倍。由此可知:
(1)写出元素符号:W为 ,X为 ,Y为 ,Z为 ;
(2)Y2Z是由 键组成的物质,其电子式为 ;
(3)由Y、X、W组成的物质中有 键和 键,形成的是 化合物;
(4)用电子式表示Z与钙形成化合物的过程 。
(1) H O Na S (2)离子键 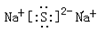 (3)离子 共价 离子 (4)
(3)离子 共价 离子 (4) 
Z元素的最高正化合价为+6,所以Z是硫元素。Y和W的最外层电子数相等,因此Y和W属于同一主族。因为只有Y为金属元素,所以Y如果是镁,则W是Be,不正确。如果Y是Al,则W是B。则不能满足Y、Z两元素原子的质子数之和为W、X两元素质子数之和的3倍。所以Y只能是钠,W是氢元素,X是氧元素。钠和硫分别是活泼的金属和活泼的非金属,形成的化学键是离子键。由H、O、Na形成的化合物是氢氧化钠,含有离子键和极性键,属于离子化合物。钙是活泼的金属元素,所以和硫形成的化合物硫化钙是由离子键形成的离子化合物。
