小明发现家中施用的碳酸氢铵(NH4HCO3)减少了,并闻到一股刺激性的气味.他很好奇,于是和同学们进行探究,请你一同参与:
[提出问题]碳酸氢氨减少的原因是什么?
[猜想假设]碳酸氢铵受热易分解,产物可能为水、二氧化碳、氨气.
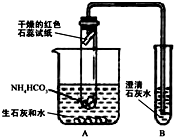
[实验设计]小明设计了如图所示的装置进行实验 (实验装置中的铁架台省略).
(1)A装置大烧杯中的生石灰和水的作用是______.
(2)装置B中澄清石灰水______,证明产物中有二氧化碳生成.
(3)根据现象______,证明实验后生成了水和氨气.
(4)小红同学认为若将装置B中澄清石灰水改为NaOH溶液,再经过某实验操作,也可以证明碳酸氢铵分解后有二氧化碳生成,请你帮她设计完成实验:
| 实验步骤 | 实验现象 | 反应的方程式 |
| ______ | ______ | ______ |
[实验反思]根据以上实验,你认为化肥碳酸氢铵在保存时应注意的问题是______,在施用时注意______.
[实验设计]
(1)因为碳酸氢铵受热容易分解,生石灰溶于水能够放出大量的热促使碳酸氢铵的分解,故A装置大烧杯中的生石灰和水的作用是:生石灰和水反应放出热量,使碳酸氢铵分解;
(2)装置B中澄清石灰水变浑浊,证明产物中有二氧化碳生成;
(3)因为碳酸氢铵分解能生成水,能使干燥的红色石蕊试纸湿润;因为氨气的水溶液显碱性,能够使湿润的石蕊试纸变成蓝色;根据干燥的红色石蕊试纸变蓝,证明实验后生成了水和氨气;
(4)二氧化碳与氢氧化钠溶液反应产生碳酸钠,可以通过加入稀盐酸看是否产生气泡;或加入氯化钙等是否产生沉淀等;
| 取装置B中溶液少许,滴加稀盐酸 (或氯化钙或氢氧化钡溶液) | 产生气泡 | Na2CO3+2HCl=2NaCl+CO2↑+H2O (或Na2CO3+CaCl2=CaCO3↓+2NaCl) |
| ||
[实验反思]因为碳酸氢铵受热容易分解,所以应该存放在阴凉干燥处,避免在气温较高、日照比较强烈的中午施用.
故答案为:[实验设计](1)生石灰和水反应放出热量,使碳酸氢铵分解;(2)变浑浊;
(3)干燥的红色石蕊试纸变蓝
| 取装置B中溶液少许,滴加稀盐酸 (或氯化钙或氢氧化钡溶液) | 产生气泡 | Na2CO3+2HCl=2NaCl+CO2↑+H2O (或Na2CO3+CaCl2=CaCO3↓+2NaCl) |
[实验结论]NH4HCO3
NH3↑+H2O+CO2↑ △ .
[实验反思]避光、避热、密封 避免在气温较高、日照比较强烈的中午施用
