某化学兴趣小组在实验室发现了一瓶标签受到腐蚀(如图)的溶液,他们对此产生了兴趣.
[提出问题]这瓶溶液究竟是什么?
经过询问实验老师平时的药品保管得知,这瓶无色溶液应该是碳酸钠、碳酸氢钠、氯化钠、硫酸钠、硝酸钠中的某一种.为了确定该药品,他们首先进行了理论分析:
(1)小明根据标签上的组成元素认为一定不可能是______.
(2)小英提出,碳酸氢钠、硝酸钠也不可能,你认为她的依据是______.
为了确定该溶液究竟是剩余两种盐的哪一种,他们设计了如下实验.
[设计实验]
| 方法 | 实验操作 | 实验现象 | 实验结论 |
| 一 | 取少量样品于试管中,慢慢滴加BaCl2溶液,静置一段时间,倾去上层清液,向沉淀中继续滴加稀盐酸 | 先出现白色沉淀,后产生大量气泡 | 该瓶无色溶液是______. |
| 二 | 取该瓶溶液,慢慢滴加______溶液 | 产生气泡 | 该瓶无色溶液是Na2CO3.反应的化学方程式是______. |
| 三 | 取少量样品于试管中,慢慢滴加MgSO4溶液 | 产生______ | 该瓶无色溶液是 Na2CO3. |
| 经查阅资料得知上述五种盐里碳酸钠、碳酸氢钠的溶液呈碱性,其余三种盐的溶液呈中性,请你再设计一种实验方法,确定该溶液究竟是哪种盐. | |||
| 四 | ______ | 溶液变红 | 该瓶无色溶液是 Na2CO3. |
(3)方法二的操作有不合理之处,请指出原因:______.
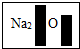
(1)氯化钠中不含有氧元素,故不可能是氯化钠;
(2)碳酸氢钠、硝酸钠的化学式中钠元素的右下角没有数字2,故不可能是碳酸氢钠和硝酸钠;
[设计实验]
方法一:根据实验的现象,加入氯化钡产生了沉淀,产生的沉淀能与盐酸反应产生气体,故该物质是碳酸钠,
方法二:碳酸钠能与盐酸反应产生气体,而硫酸钠不与盐酸反应,故可以使用盐酸,与样品混合,观察有无气体产生来确定物质的成分;
方法三:碳酸钠能够和硫酸镁反应产生碳酸镁沉淀.而硫酸钠不反应;
方法四:碳酸钠溶液呈碱性,而硫酸钠的水溶液呈中性,可以使用滴加几滴无色酚酞,观察到溶液变红验证结论;
(3)方法二的操作是“取该瓶溶液”滴加检测试剂,会将该瓶试剂全部污染,无法进行后续实验,应该取少量样品于试管中进行实验.
故答案为:(1)NaCl (2)标签化学式中Na的右下角为2;而这两种物质的化学式中Na元素的右下角不会有2;
[设计实验]
| 方法 | 实验操作 | 实验现象 | 实验结论 | |
| 一 | Na2CO3 | |||
| 二 | 盐酸 | 2HCl+Na2CO3═2NaCl+CO2↑+H2O | ||
| 三 | 白色沉淀 | |||
| 四 | 取少量样品于试管中,滴加滴加2至3滴酚酞 | |||
