(12分)X、Y、Z、W为按原子序数由小到大排列的四种短周期元素,已知:
①X元素原子价电子排布式为ns2np2,且原子半径是同族元素中最小的。
②Y元素是地壳中含量最多的元素;W在同周期中原子半径最小,在W原子的电子排布中,
p轨道上只有1个未成对电子。
③Z元素的电离能数据见下表(kJ/mol):
| I1 | I2 | I3 | I4 | …… |
| 496 | 4562 | 6912 | 9540 | …… |
(1)Z2Y2的电子式为___________, Z2Y2与水反应的化学方程式
(2)X、Y二种元素所形成的常见稳定的化合物的晶体类型为________ ,空间构型为________
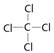
(3)X、Y、Z、W四种元素所形成的单质中,硬度最大、熔点最高的是_____________ (填名称); XW4的结构式为_______________
(每空2分共12分)
(1) 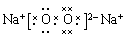
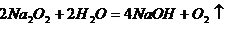
(2) 分子晶体 直线形 (3)金刚石 
根据①可知X是第ⅣA元素,因此是碳元素。地壳中含量最高的是氧元素,则Y是氧元素。根据Z的电离能可知,Z是第IA元素。又因为Z的原子序数大于氧元素的,所以Z是短周期中的钠元素。同周期元素中原子半径最小的是第ⅦA元素。又因为W原子序数大于钠的,所以W是氯元素。
(1)过氧化钠是含有离子键和非极性键的离子化合物,和水反应生成氢氧化钠和氧气。
(2)碳元素的稳定氧化物是CO2,由于碳原子没有孤对电子,所以是直线型结构,属于分子晶体。
(3)金刚石是原子晶体,熔沸点最高。结构式是指用1根短线表示一对电子对的式子,所以四氯化碳的结构式为