高温下赤热的焦炭能与水蒸气发生反应生成无色的气体,探究小组同学对其反应后生成的气体作了如下探究:
【猜想与假设】假设①:生成的气体可能有H2、CO;
假设②:生成的气体可能有H2、CO2、______;
假设③:生成的气体可能有H2、CO、CO2、N2;
假设④:组长认为③的猜想不合理,他作出判断的理论依据是______.
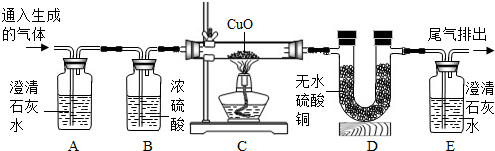
【设计与实验】为了证明他们的猜想是正确的,设计了如图所示的实验装置:
(提示:浓硫酸作干燥剂,无水硫酸铜遇到水变蓝色,H2和CuO反应生成Cu和H2O,CO与CuO反应的原理与工业炼铁的反应原理相似.)
①证明混合气体中含有H2,相应的反应现象是______
②证明混合气体中含有CO,相应的反应现象是______
③证明混合气体中含有CO2,相应的反应现象是______
【结论与思考】实验后得出结论,假设①成立.
①写出焦炭与水蒸气发生反应的化学方程式______;
②有同学认为尾气直接排出会污染空气,应如何处理更合理:______
(1)在化学反应前后,元素的种类是不发生改变的,依据反应物是碳和水,所以生成的气体可能有H2、CO2、CO;反应前的物质中没有氮元素,生成物中也不会有氮元素,所以水和碳反应后不会生成氮气,
(2)①水能够使无水硫酸铜变蓝,氢气和氧化铜反应会生成水,只要D中的无水硫酸铜变蓝,就证明水的存在,也证明了混合气中有氢气;
②二氧化碳能使澄清石灰水变浑浊,一氧化碳和氧化铜反应会生成二氧化碳,只要澄清石灰水变浑浊,证明了二氧化碳的存在,也证明了混合气中有一氧化碳;
③二氧化碳能使澄清石灰水变浑浊,根据石灰水变浑浊的现象,可以确定混合气体中存在二氧化碳;
(3)①根据焦炭和水在高温条件下生成氢气和一氧化碳,化学方程式为:C+H2O
CO+H2; 高温 .
②因为一氧化碳有毒,不能直接排入大气中,可以在导管口点燃一个酒精灯使一氧化碳燃烧生成无污染的二氧化碳,或收集处理;
故答案为:
【猜想与假设】CO; 反应物中没有N元素,根据质量守恒定律不可能生成N2;
【设计与实验】①D中无水硫酸铜变蓝色; ②E中澄清石灰水变浑浊; ③A中澄清石灰水变浑浊;
【结论与思考】①C+H2O
H2+CO; ②在尾气排出处加一盏点燃的酒精灯或用空的气囊收集(合理均可). 高温 .
