氢氧化钠与酸、二氧化碳反应没有明显现象.小军和小晴两位同学想用实验证明氢氧化钠能与盐酸、二氧化碳反应,他们做了以下探究过程.
查阅资料:通常状况下,1体积水能溶解1体积二氧化碳.
设计实验:小军设计了两个实验进行验证,请你帮他完成下列实验报告.
| 实验操作 | 实验现象 | 实验结论及解释 | |
| 1 | NaOH溶液酚酞试液盐酸过量 | ______ ______ | 氢氧化钠可以与盐酸反应. 该反应的化学方程式为: ______ |
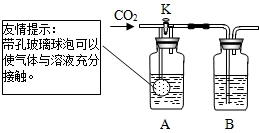
| ② | 小军选用NaOH和Ca(OH)2两种溶液分别放入上边装置中的广口瓶中,关闭K,通入二氧化碳.
| A、B中均无明显变化. | B中盛放的溶液是______. 该实验目的是______ ______. |
(1)小军的第一个实验的缺陷是______,应改为______.
(2)小晴用上述小军第二个实验的装置和药品,验证氢氧化钠可以与二氧化碳反应,她的设计方案是:分别量取40mLNaOH和Ca(OH)2溶液放入A、B中,______,此实验可以说明氢氧化钠和二氧化碳发生了反应.
实验结论:通过小晴的实验,证明了氢氧化钠可以与盐酸和二氧化碳反应.
(1)酚酞试液遇酸也不变色,为无色;为证明酚酞试液又变无色是由于氢氧化钠与盐酸反应的结果应加入适量的盐酸;
(2)已知“通常状况下,1体积的水约能溶解1体积二氧化碳”,则量取40ml上述溶液放入A,最多溶解40ml二氧化碳,剩余的二氧化碳一定与氢氧化钠溶液反应,而无剩余的二氧化碳再与氢氧化钙反应,所以“A、B中均无明显变化”,此实验可以说明二氧化碳和氢氧化钠发生了反应,其理由是关闭K时,B中溶液无明显变化,且通入的二氧化碳体积远大于A中溶液的体积,说明二氧化碳和氢氧化钠发生了反应.
故答案为:(1)用过量的盐酸、适量的盐酸
(2)关闭K时,B中溶液无明显变化,且通入的二氧化碳体积远大于A中溶液的体积,说明二氧化碳和氢氧化钠发生了反应