有一种神奇的蜡烛,如图1,点燃后任你怎么吹也吹不灭,而且看上去和普通的蜡烛一模一样,那么到底是什么玄机能让蜡烛持续燃烧?两根银白色的金属丝的成分是什么呢?请你一起参与探究.
(1)查阅资料:普通蜡烛由石蜡和蜡烛芯制成的,而吹不灭的蜡烛的棉芯里藏了两根相互缠绕的银白色金属丝,它的着火点只有150℃.当蜡烛燃烧时,金属并不燃烧;但当蜡烛吹灭后,未冷却的金属接触到氧气就发生燃烧,从而使蜡烛复燃.
探究与反思:
这种蜡烛燃烧时,蜡烛芯里的金属为什么不燃烧?______;这种蜡烛也可以熄灭,你采用的方法是______.
(2)对两根金属丝的成分的探究.
老师指出金属丝的成分可能是Mg、Al、Fe中的一种或两种.回校后,老师提供了Mg、Al、Fe三种已知金属和MgSO4、Al2(SO4)3、FeSO4、CuSO4四种盐溶液(已知MgSO4、Al2(SO4)3溶液无色,FeSO4溶液为浅绿色,CuSO4溶液为蓝色)以及未知金属的样品.指导同学们先进行了参照实验,之后探究未知金属的成分.
①三种已知金属的参照实验
| 试剂 | Mg | Al | Fe |
| MgSO4溶液 | 有气泡产生. | ▲ | ▲ |
| Al2(SO4)3溶液 | 有大量气泡产生,一段时间后金属表面有白色固体附着. | ▲ | ▲ |
| FeSO4溶液 | 有大量气泡产生,一段时间后金属表面有灰黑色固体附着. | 试管底部有灰黑色固体析出. | ▲ |
| CuSO4溶液 | 有大量气泡产生,一段时间后金属表面有红色固体附着. | 一段时间后金属表面有红色固体附着. | 一段时间后金属表面有红色固体附着. |
②未知金属成分的探究
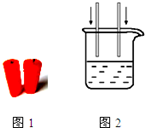
该小组同学将两根未知金属丝分开,如图2所示放入CuSO4溶液中,观察到的现象记录如下:
| 试剂 | 两根未知金属丝 |
CuSO4溶液 | 一根金属丝上有大量气泡产生,另一根金属丝上没有气泡;一段时间后,两根金属丝表面都有红色固体附着. |
③实验反思
同学们在反思实验原理时,提出还可将另一种金属直接放入稀硫酸或稀盐酸中,有的同学认为可以通过“金属产生气泡的快慢”这一现象进行判断,有的同学认为这种判断依据不够合理,理由是______.但是“将另一种金属直接放入稀硫酸中”还是可以判断出金属的成分,依据的现象是______.
(1)蜡烛燃烧时,氧气与石蜡反应,而使蜡烛芯里的金属接触不到充足的氧气,所以不燃烧;要想使其熄灭可控制燃烧的条件完成,例如隔绝氧气或剪除灯芯或用水浇灭等;
(2)①金属与盐反应时金属必须排在盐中金属的前面,根据金属活动性顺序可知,“▲”标记的实验都是不反应的所以实验现象是无明显变化;铝和硫酸亚铁溶液反应生成硫酸铝和铁,所以表中的“灰黑色固体”的成分为铁粉;
②一根金属丝上有大量气泡产生,根据三种已知金属的参照实验现象可知,只有镁能产生气泡;根据铝与铁与其他物质反应的现象不同来区分,由三种已知金属的参照实验现象可知与硫酸亚铁反应现象不同,所以在试管中加入FeSO4溶液,将另一根金属丝插入其中.若金属丝上无明显变化,则证明该金属丝是铁丝;若一段时间后试管底部有灰黑色固体析出,则证明该金属丝是铝丝;
③金属产生气泡的快慢需要通过对比实验才能看出,未知金属只有一种,不能设计金属对比实验;由于硫酸与铝反应现象是有气泡产生,铁与硫酸反应有气泡,且溶液为浅绿色.
故答案为:(1)蜡烛燃烧时,氧气与石蜡反应,而使蜡烛芯里的金属接触不到充足的氧气,所以不燃烧;用水浇灭(或者在火焰上方罩一烧杯);
(2)①无明显变化;铁粉;②Mg;将金属丝插入Al2(SO4)3溶液(或者FeSO4溶液)中;
③未知金属只有一种,没有用参照金属对比,无法判断金属的种类(或无法判断反应速率的快慢);溶液是否变成浅绿色.
