问题
填空题
W、X、Y、Z是短周期元素,它们的核电荷数依次增大。下表列出它们的性质和结构:
| 元素编号 | 元素性质或原子结构 |
| W | 原子电子层数与核外电子数相等 |
| X | 核外S能级上的电子总数与P能级上的电子总数相等 |
| Y | 元素的原子半径在该周期中最大(除稀有气体外) |
| Z | 原子核外P能级上的电子总数比S能级上的电子总数多2 |
⑵Y元素原子的核外最外层电子排布式为____________。
⑶W和X形成的化合物的电子式________________,该化合物为________分子(填“极性”或“非极性”)。Z和X形成的化合物构成的晶体属于__________晶体。
⑷Y元素的单质在W和X形成的化合物中反应的化学方程式为______________________________。
答案
(共8分)(1)O、 Si (各1分) (2)3s1 (1分)
(3) 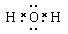 极性 原子(各1分) (4)2Na+2H2O=2NaOH+H2↑(2分)
极性 原子(各1分) (4)2Na+2H2O=2NaOH+H2↑(2分)
根据元素的性质及结构特点可知,W是H,X是O,Y是Na,Z是Si。
(1)略
(2)根据构造原理可知,Y元素原子的核外最外层电子排布式为3s1。
(3)H和O形成的水,含有极性键的极性分子,电子式为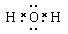 。Z和X形成的化合物是二氧化硅,属于分子晶体。
。Z和X形成的化合物是二氧化硅,属于分子晶体。
(4)钠是活泼的金属,极易和水反应,生成氢氧化钠和氢气,反应式为2Na+2H2O=2NaOH+H2↑。
