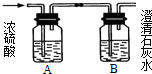
如图所示,某气体X可能由H2、CO、CH4中的一种或几种组成.将X气体充分燃烧,将燃烧后生成的气体分别通过A、B两个洗气瓶.试回答下列问题:
(1)若A洗气瓶的质量增加了3.8 g,B洗气瓶的质量不变,则气体X是______.
(2)若A、B两个洗气瓶的质量分别增加了3.8 g和4.4 g,则气体X中可能含有①______,②______,③______.
(1)若A洗气瓶的质量增加了3.8 g,B洗气瓶的质量不变,说明只生成了水,故X气体是氢气.
(2)若A、B两个洗气瓶的质量分别增加了3.8 g和4.4 g,说明生成3.8g水和4.4g二氧化碳,根据水和二氧化碳得到质量可以计算出反应物中C和H的质量比,从而可以确定X气体的组合.3.8g水中所含氢元素的质量为:3.8g×
═2 18
g;4.4g二氧化碳中碳的质量为:4.4g×19 45
=1.2g;则H:C=19:54.由此可推出X不可能为甲烷,也不能为甲烷和一氧化碳的混合气体.12 44
答:(1)H2
(2)①CH4、H2 ②CO、H2 ③CH4、CO、H2
