(10分)有A、B、C、D、E五种短周期元素, 它们的原子序数由A到E依次增大, 已知A和B、C原子有相同的电子层数, 且A的L层电子数是K层电子数的两倍,D燃烧时呈现黄色火焰, D的单质在高温下与C的单质充分反应, 可以得到与E单质颜色相同的淡黄色固态化合物, 试根据以上叙述回答:
(1)写出元素符号: A B C D
(2)写出B的最高价氧化物对应水化物与最低价的氢化物反应的化学方程式
(3)用电子式表示化合物 D2E 。
(4)B和C的氢化物中,稳定性较弱的是________ (选填B或C);D和E的离子中,半径较小的是________ (填离子符号)。
(5)元素E在元素周期表中的位置是 ;
(1)C、N、O、Na (2)HNO3+NH3=NH4NO3
(3)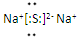 (4)B;Na+ (5)第3周期VIA
(4)B;Na+ (5)第3周期VIA
(1)根据元素的结构及性质可知,A、B、C、D、E五种短周期元素分别是C、N、O、Na、S。
(2)两种物质分别是和硝酸和氨气,方程式为HNO3+NH3=NH4NO3。
(3)硫化钠是含有离子键的离子化合物,电子式为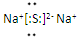 。
。
(4)非金属性越强,相应氢化物的稳定性越强。非金属性是N大于C,所以B的氢化物稳定性差。硫离子有3个电子层,而钠离子有2个,所以离子半径较小的是Na+。
(5)S的原子序数是16,位于第3周期VIA 。
