(9分)短周期主族元素A、B、C、D、E在元素周期表中的位置如图所示。请回答下列问题:
| B | C | D | ||
| A | E |
(2)E的氢化物与其最高价氧化物对应水化物的钾盐共热能发生反应,生成一种气体单质。反应的化学方程式为 ;
(3)C有多种氧化物,其中甲的相对分子质量最小,在一定条件下2L甲气体与0.5L氧气相混合,若该气体混合物被足量的NaOH溶液完全吸收后没有气体残留,所生成的含氧酸盐的化学式是 ;
(4)在298K下,A、B的单质各1 mol 完全燃烧,分别放出热量aKJ和bKJ,又知一定条件下,A的单质能将B从它的最高价氧化物中置换出来。若此置换反应生成3mol B的单质,则该反应在298K下的△H (注:题中所设单质的为稳定单质)。
(5)要证明与D同主族且相邻的元素的非金属性与E的非金属性强弱,正确、合理的实验操作及现象是 。
(1)O>N>C (2)8HCl+KClO4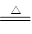 KCl+4Cl2↑+4H2O
KCl+4Cl2↑+4H2O
(3)NaNO2 (4)-(4a-3b)KJ/mol 或 (3b-4a)KJ/mol
(5)将氯水(或氯气)滴入(通入)硫化钠(或硫氢化钠)溶液中,有淡黄色沉淀生成
题目分析:根据元素周期表的结构可知B为C,C为N,D为O,A为Al,E为Cl。
(1)根据同周期从左往右非金属性依次增强判断,非金属性O>N>C。
(2)盐酸与高氯酸钾反应的方程式为8HCl+KClO4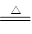 KCl+4Cl2↑+4H2O。
KCl+4Cl2↑+4H2O。
(3)氮的氧化物中相对分子质量最小的是NO,2LNO与0.5L氧气混合得到1LNO2和1LNO的混合气体,被足量的NaOH吸收气体无残留,因此发生了归中反应,生成NaNO2。
(4)①4Al(s)+3O2(g)=2Al2O3(s) ΔH=-4akJ/mol ②C(s)+O2(g)=CO2(g) ΔH=-bkJ/mol,可知反应4Al(s)+3CO2(g)=3C(s)+2Al2O3(s)的反应热ΔH为①-3②=(3b-4a)KJ/mol。
(5)证明非金属强弱可以用非金属性强的将非金属性弱的置换出来,所以将氯气通入到硫化钠溶液中,有淡黄色的沉淀生成。
点评:该题以“周期表中元素的推断”为载体,考查学生对元素周期表的熟悉程度及其对表中各元素性质和相应原子结构的周期性递变规律的认识和掌握程度。考查了学生对物质结构与性质关系以及运用所学的知识解决具体化学问题的能力。本题基础性较强,属于中等难度的试题。
