问题
填空题
(7分)X、Y、Z三种常见元素的单质,甲、乙是两种常见的化合物,相互间有如右图转化关系。
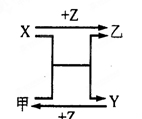
回答下列问题:
(1) 若X基态原子外围电子排布式为3s2,甲是由第二周期两种元素的原子构成的非极性气态分子, Y原子的基态轨道表示式为 ,乙的电子式为 。
(2) 若X基态原子外围电子排布式为3s1,Y具有许多优越的性能,被称为未来金属,甲中共含有90个电子,则其分子式为 ,Y的电子排布式为 。
(3) 若X、Y均为金属单质,X基态原子外围电子排布式为3s23p1,甲为具有磁性的黑色固体,则X与甲反应的化学方程式为: ,Y原子基态电子排布式为 。
答案
7分)(1)1s22s22p2;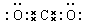
(2)TiCl4 ;3d24s2 (3)3Fe3O4+8Al 9Fe+4Al2O3 ; 3d64s2
9Fe+4Al2O3 ; 3d64s2
(1) 若X基态原子外围电子排布式为3s2,则X是镁。甲是由第二周期两种元素的原子构成的非极性气态分子,则甲是CO2,所以Y是碳,乙是氧化镁,因此Z是氧气。
(2) 若X基态原子外围电子排布式为3s1,则X是Na。被称为未来金属的是钛,即Y是Ti。又因为甲中共含有90个电子,所以甲应该是TiCl4 。因此Z是氯气,乙是氯化钠。
(3)X基态原子外围电子排布式为3s23p1,则X是Al。甲为具有磁性的黑色固体,所以甲是四氧化三铁,则Y是铁,Z是氧气,乙是氧化铝。

 I'm a boy. I'm from China.
I'm a boy. I'm from China. I'm a girl. I'm a student.
I'm a girl. I'm a student. I'm a girl. I'm a teacher.
I'm a girl. I'm a teacher. I'm from Canada. I'm a teacher.
I'm from Canada. I'm a teacher. We're from America. We're students.
We're from America. We're students.