(10分)下表为元素周期表的一部分,请回答有关问题:
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 4 | ⑨ | ⑩ |
(2) ③④⑤原子半径由大到小的顺序是______________________(填元素符号)
(3) 表中最活泼的金属是_________,非金属性最强的元素是________;(填写元素符号)
(4) 表中能形成两性氢氧化物的元素是__________,写出该元素的氢氧化物与⑨的最高价氧化物对应水化物反应的离子方程式:
______________________________________________________________________。
(5) 用电子式表示③与⑥的化合物的形成过程:
______________________________________________________________________。
(1)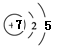 溴 (2)Mg>Al>Si (3) K F
溴 (2)Mg>Al>Si (3) K F
(4) Al Al(OH)3+ OH—= AlO2—+ 2H2O
(5) 
(1)①是氮元素,原子结构示意图为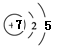 ;⑩是Br,名称是溴。
;⑩是Br,名称是溴。
(2)同周期自左向右,原子半径逐渐减小,所以应该是Mg>Al>Si。
(3)同周期自左向右金属性逐渐减弱,非金属性逐渐增强;同主族自上而下金属性逐渐增强,非金属性逐渐减弱,所以金属性最强的是K。非金属性最强的F。
(4)氢氧化铝是两性氢氧化物,和氢氧化钠反应的方程式为Al(OH)3+ OH—= AlO2—+ 2H2O。
(5)③与⑥分别是Mg和S,形成的化学键是离子键,所以形成过程为 。
。
