如图表示的是一个化合物的组成分析实验.
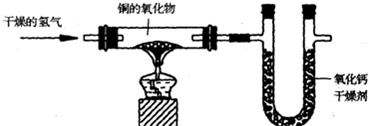
| 实验前 | 实验后 | |
| 铜的氧化物+玻璃管* | 137.8g | 131.4g |
| 氧化钙十U形管 | 100.8g | 108g |
试根据实验数据求:
(1)完全反应后生成水的质量______.
(2)生成的水中氧的质量______.
(3)铜的氧化物中铜的质量______.
(4)铜的氧化物中铜和氧的质量比______.将化合物组成元素的质量比,分别除以各自的原子量,即可求得该化合物中各元素的原子个数比______.
(5)计算铜的氧化物中铜、氧的原子个数比______.
(6)将(5)的计算结果变为最简整数比,即求得铜的氧化物的化学式.试写出铜的氧化物的化学式______.
(1)完全反应生成的水,由于被干燥剂氯化钙所吸收,因此水的质量为:108.0g-100.8g═7.2g,故答案为:7.2g;
(2)铜的氧化物减少的质量即被夺走得氧元素的质量,即是生成的水中所含氧元素的质量,所以水中氧元素的质量:137.8g-131.4g=6.4g;
(3)铜的氧化物减少的质量即被夺走得氧元素的质量,氧化铜的质量减去氧元素的质量即是铜元素的质量,为:137.8g-80.2g-6.4g=51.2g;
(4)铜的氧化物中有氧元素6.4g,铜元素51.2g,因此铜、氧元素的质量比为:51.2g:6.4g=8:1;则铜的氧化物中铜、氧的原子个数比是:
:8 64
=2:1;1 16
(5)根据题意:将化合物组成元素的质量比,分别除以各自的原子量,即可求得该化合物中各元素的原子个数比.则铜的氧化物中铜、氧的原子个数比是:
:8 64
=2:1;1 16
(6)铜的氧化物中铜、氧的原子个数比是:
:8 64
=2:1,因此该氧化物是Cu2O;1 16
故答案为:
(1)7.2g;(2)6.4g;(3)51.2g;(4)8:1;2:1(5)2:1;(6)Cu2O.
