问题
填空题
(7分)根据下表信息回答以下问题:部分短周期元素的原子半径及主要化合价。
| 元素 | A | B | C | D |
| 原子半径(nm) | 0.130 | 0.118 | 0.090 | 0.102 |
| 主要化合价 | +2 | +3 | +2 | +6,-2 |
| 元素 | E | F | G | H |
| 原子半径(nm) | 0.073 | 0.154 | 0.037 | 0.099 |
| 主要化合价 | -2 | +1 | +1 | +7,-1 |
(2)B、H两元素的最高价氧化物所对应的水化物相互反应的离子方程式是________。
(3)实验室中制取H单质反应的化学方程式是________。
(4)将A、B两种元素的单质用导线连接浸入NaOH溶液中,发现导线中有电流产生,其负极反应式为________。
答案
(1)离子键和共价键 (2)Al(OH)3+3H+===Al3++3H2O
(3)MnO2+4HCl(浓)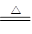 MnCl2+Cl2↑+2H2O (4)Al-3e-+4OH-===AlO2-+2H2O
MnCl2+Cl2↑+2H2O (4)Al-3e-+4OH-===AlO2-+2H2O
根据元素的结构及有关性质可知,A是Mg,B是Al,C是Be,D是S,E是O,F是Na,G是H,H是Cl。
(1)E、F、G三元素形成的化合物是氢氧化钠,含有离子键和极性键。
(2)B、H两元素的最高价氧化物所对应的水化物分别是氢氧化铝和高氯酸,所以二者反应的方程式是Al(OH)3+3H+===Al3++3H2O。
(3)实验室制取氯气的化学方程式是MnO2+4HCl(浓)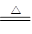 MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。
(4)镁的活泼性强于铝的,但镁和氢氧化钠溶液不反应,而铝是可以反应的,所以铝是负极,镁是正极。则负极电极反应式是Al-3e-+4OH-===AlO2-+2H2O。