(7分)请根据表格回答问题:
(ⅰ)根据下 * * 种元素的电离能数据(单位:kJ/mol),回答下面各题。
| 元素代号 | I1 | I2 | I3 | I4 |
| E | 500 | 4600 | 6900 | 9500 |
| F | 740 | 1500 | 7700 | 10500 |
| H | 580 | 1800 | 2700 | 11600 |
| I | 420 | 3100 | 4400 | 5900 |
A.F和H B.H和I C.E和H D.E和I
(2)它们的氯化物的化学式,最可能正确的是( )
A.ECl B.FCl3 C.HCl D.ICl4
(3)F元素最可能是( )
A.S区元素 B.稀有气体元素 C.p区元素 D.准金属 E.d区元素
(ⅱ)右表是元素周期表的一部分:
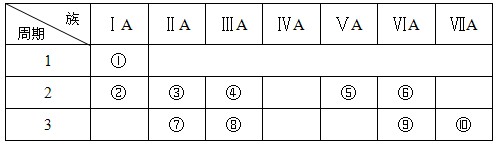
(4)某元素原子的核外p电子数比s电子数少1,则该元素的元素符号是
其原子的结构示意图是 。
(5)已知某些不同族元素的性质也有一定的相似性,如元素③与元素⑧的氢氧化物有相似的性质。这种现象被称为 。
(6)又如表中与元素⑦的性质相似的不同族元素是 (填元素符号)。
(1)D (2)A (3)A (4) N 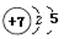 (5) 对角线规则 (6)Li
(5) 对角线规则 (6)Li
(1)根据表中电离能的数据可知,E和I的第二电离能远大于低于电离能,所以均是第IA元素;而F应该是第ⅡA元素,H应该是ⅢA元素,所以答案选D。
(2)根据元素所在的族序数可知,E、F、H、I分别应该是ECl、FCl2、HCl3、ICl,所以答案选A。
(3)由于F是第ⅡA元素,所以F是S区元素,答案选A。
(4)根据构造原理可知,如果元素原子的核外p电子数比s电子数少1,则该元素一定是氮元素,其原子结构示意图是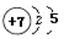 。
。
(5)根据元素在周期表中的位置可知,③和⑧处于对角线位置,所以这种现象被称为对角线规则。
(6)⑦是镁元素和Li元素处于对角线位置,二者的性质是相似的。
