(共13分)A、B、C、D、E、F、G、L、I九种主族元素分布在三个不同的短周期,它们的原子序数依次增大,其中B、C、D为同一周期,A与E、B与G、D与L分别为同一主族,C、D、F三种元素的原子序数之和为28,F的质子数比D多5,D的最外层电子数是F的2倍,C和D的最外层电子数之和为11。请回答下列问题:
(1)以上八种元素中非金属所形成的最简单气态氢化物稳定性最弱的是(填化学式)____________,E、F、L所形成的简单离子的半径由大到小的顺序为(用离子符号表示)__ __ > > 。
(2)由L、I两元素可按原子个数比1:1组成化合物X,化合物X中各原子均满足8电子的稳定结构,则X的电子式为 。固体化合物E2D2投入到化合物E2L的水溶液中,只观察到有沉淀产生的,写出该反应的离子方程式为: 。
(3)在10 L的密闭容器中,通入2mol LD2气体和1 mol D2气体,一定温度下反应后生成LD3气体,当反应达到平衡时,D2的浓度为0.01 mol·L-1,同时放出约177 kJ的热量,则平衡时LD2的转化率为 ;该反应的热化学方程式为 ;此时该反应的平衡常数K= 。
(4) 有人设想寻求合适的催化剂和电极材料,以C2、A2为电极反应物,以HCl—NH4Cl溶液为电解质溶液制造新型燃料电池,试写出该电池的正极反应式 ;
(共13分)(1)SiH4(1分) S2-﹥ Na+ ﹥ Al3+ (1分)
(2) 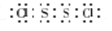 (2分)Na2O2+ S2-+2 H2O="=S+2" Na++4OH- (2分)
(2分)Na2O2+ S2-+2 H2O="=S+2" Na++4OH- (2分)
(3)90% (1分) 2SO2 (g)+O2 (g)  2SO2 (g) ΔH=-196.7 kJ·mol-1 (2分)8100(2分)
2SO2 (g) ΔH=-196.7 kJ·mol-1 (2分)8100(2分)
(4) N2 + 6e-+ 8H+==2NH4+(2分)
题目分析:F的质子数比D多5,D的最外层电子数是F的2倍,则D应该是第二周期元素,F应该是第三周期元素。设F的最外层电子数是x,则D的最外层电子数就是2x,因此有关系式10+x-2-2x=5,解得x=3,则D是氧元素,F是Al。C、D、F三种元素的原子序数之和为28,因此C的原子序数是28-8-13=7,即C是氮元素。D与L属于同主族,且L的原子序数大于D的,因此L是S元素,I的原子序数最大,则I是氯元素。由于九种主族元素分布在三个不同的短周期,所以A是氢元素。A与E同主族,则根据E的原子数大于氧元素的可知,E是Na。G的原子序数只能是14或15,则根据B和G属于同主族且B的原子序数小于氮元素的可知,G不是P,应该是Si。则B是碳元素。
点评:本题主要是元素“位、构、性”三者关系的综合考查,比较全面考查学生有关元素推断知识和灵活运用知识的能力。该题以“周期表中元素的推断”为载体,考查学生对元素周期表的熟悉程度及其对表中各元素性质和相应原子结构的周期性递变规律的认识和掌握程度。考查了学生对物质结构与性质关系以及运用元素周期律解决具体化学问题的能力。:
