(10分)下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题:
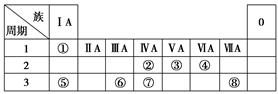
(1)③、④、⑤的原子半径由大到小的顺序是____________________。
(2)②、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是________________。
(3)①、②、④、⑤四种元素可形成中学常见的化合物M,写出M中存在的化学键类型_______;加热M固体可生成一种酸性氧化物,写出此氧化物的电子式______________________。
(4)由表中①④两种元素的原子按1∶1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为(填序号)________。
a.MnO2 b.Na2SO3 c.FeCl3 d.KMnO4
(1)Na>N>O
(2)HClO4>H2CO3>H2SiO3
(3)既含离子键又含极性共价键 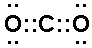
(4)ac
题目分析:根据元素所在周期表中的位置,可知元素的种类,①为H元素,②为C元素,③为N元素,④为O元素,⑤为Na元素,⑥为Al元素,⑦为Si元素,⑧为Cl元素。
(1)Na与Al同周期,周期表中,同周期元素从左到右原子半径逐渐减小,则原子半径Na>Al,原子核外电子层数越多,半径越大,则有原子半径Na>Al>O。
(2)②、⑦、⑧对应的元素分别为C、Si、Cl,非金属性:Cl>C>Si,元素的非金属性越强,对应的最高价含氧酸的酸性越强,则HClO4>H2CO3>H2SiO3;
(3))①、②、④、⑤对应的元素分别为H、C、O、Na,形成NaHCO3离子化合物,既含离子键又含极性共价键;CO2的电子式要注意碳要形成四个共用电子对;
(4)H2O2在MnO2或FeCl3催化作用下分解,而Na2SO3具有还原性,与H2O2发生氧化还原反应,不能用作催化剂,高锰酸钾具有强氧化性,与H2O2发生氧化还原反应,也不能作催化剂。
点评:本题题目难度不大,根据元素在周期表中的物质可推断出元素的种类,题中侧重于周期律的应用,学习中注意积累相关知识,把握电子式的书写。
