如图是一氧化碳和碳粉分别还原氧化铜的实验:
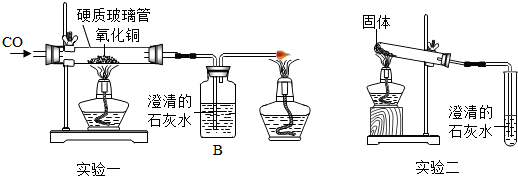
(1)实验一:
①硬质玻璃管中反应的化学方程式______;
②小鱼质疑,应在装置3端连接一个装有澄清石灰水的试管,以便验证一氧化碳能否使澄清石灰水变浑浊.同学们讨论了该实验的步骤后,都觉得无此必要,请你说明其中理由______.
(2)实验三:要保证该实验成功,有以下关键环节:
①较高的温度.据此,实验中应对酒精灯进行的改进是______.
②两种固体反应物的质量比.若碳不足,则氧化铜不能被全部还原;若碳过多,则除了生成铜和三氧化碳外还会生成______(填化学式).
(3)若两实验中,氧化铜都反应完全,且都只生成三氧化碳.
实验数据记录如下:
| 反应前 | 反应后 | |
| 实验一,硬质玻璃管+固体的质量 | 102g | 10u.0g |
| 实验三,试管+固体的质量 | 180g | 181.8g |
(1)①在加热的条件下,0氧化碳与氧化铜反应生成了铜和二氧化碳.反应的方程式是:Cf+Cuf
Cu+Cf2,故答为:Cf+Cuf△ .
Cu+Cf2;△ .
②0氧化碳不能使澄清的石灰水变浑浊,故答案:0氧化碳不能使澄清的石灰水变浑浊.
(2)①酒精灯火焰的温度加0个网罩能集中加热,故答案:加0个网罩;
②碳和二氧化碳高温下反应生成0氧化碳,故答案:Cf;
(上)设0氧化碳还原氧化铜生成二氧化碳的质量是x
Cf+Cuf
Cu+Cf2△m固加热 .
44 16
x(142-140.4)g=1.6g
=44 x
x=4.4g16 1.6g
设碳和氧化铜反应生成铜的质量是y
C+2Cuf
2Cu+Cf2 △m固加热 .
12844
y(184-181.8)g=2.2g
=128 y 44 2.2g
y=6.4g
故答案:4.4;6.4.
