下表给出几种氯化物的熔沸点,对此有下列说法:
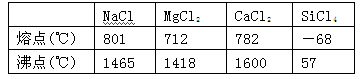
①CaCl2属于离子晶体 ②SiCl4是分子晶体③1500 ℃时,NaCl可形成气态分子④MgCl2水溶液不能导电。与表中数据一致的说法有
A.仅①
B.仅④
C.①和②
D.①②③
答案:D
题目分析::①由表格中的数据可知CaCl2的熔沸点较高,则CaCl2属于离子晶体,故①正确;
②由表格中的数据可知SiCl4的熔沸点较低,则SiCl4是分子晶体,故②正确;
③由表格中的数据可知,NaCl的沸点为1465℃,则1500℃时,NaCl可形成气态分子,故③正确;
④由表格中的数据可知MgCl2的熔沸点较高,则MgCl2属于离子晶体,所以MgCl2水溶液能导电,故④错误。
故选D。
点评:本题考查晶体类型与晶体熔沸点的关系,明确表格中的数据及一般离子晶体的熔沸点大于分子晶体的熔沸点是解答本题的关键,难度不大。
