现有部分短周期元素的性质或原子结构如下表:
| 元素编号 | 元素性质或原子结构 |
| A | 有三个电子层,且K、M层电子数之和等于L层电子数 |
| B | 最外层电子数是次外层电的2倍 |
| C | 常温下单质为双原子分子,其氢化物的水溶液呈碱性 |
| D | 元素最高正价是+7价 |
(2)写出C元素的单质的电子式 。
(3)元素D与元素A相比,非金属性较强的是 (用元素符号表示),下列表述中 能证明这一事实的是 (填选项序号)。
a.常温下D的单质和A的单质状态不同
b.D的氢化物比A的氢化物稳定
c.一定条件下D和A的单质都能与钠反应
(4)探寻物质的性质差异性是学习的重要方法之一。A、B、C、D四种元素的最高价氧化物 的水化物中化学性质明显不同于其他三种的是 (写化学式)。
(每空1分,共6分)(1)第三周期第ⅥA族 ;碳
(2)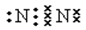 (3) Cl b (4)H2CO3
(3) Cl b (4)H2CO3
题目分析:(1)有三个电子层,且K、M层电子数之和等于L层电子数,则A是S元素,位于第三周期第ⅥA族。最外层电子数是次外层电的2倍,则B是碳元素。常温下单质为双原子分子,其氢化物的水溶液呈碱性,所以C是氮元素。元素最高正价是+7价,则在短周期元素中是氯元素。
(2)氮气中含有三键,电子式为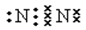 。
。
(3)同周期自左向右,非金属性逐渐增强,所以氯元素的非金属性强于S元素的非金属性。非金属性越强,氢化物的稳定性越强,则答案选b。
(4)四种元素的最高价氧化物的水化物的酸性除了碳酸是弱酸外,强于都是强酸,即A、B、C、D四种元素的最高价氧化物 的水化物中化学性质明显不同于其他三种的是H2CO3。
点评:该题是中等难度的试题,试题基础性强,贴近高考。本题主要是元素“位、构、性”三者关系的综合考查,比较全面考查学生有关元素推断知识和灵活运用知识的能力。该题以“周期表中元素的推断”为载体,考查学生对元素周期表的熟悉程度及其对表中各元素性质和相应原子结构的周期性递变规律的认识和掌握程度。考查了学生对物质结构与性质关系以及运用元素周期律解决具体化学问题的能力。
