问题
问答题
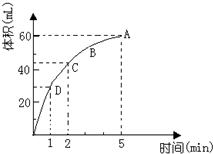
为了研究MnO2与双氧水(H2O2)的反应速率,某学生加入少许的MnO2粉末于 50mL密度为 1.1g/cm3的双氧水溶液中,通过实验测定:在标准状况下放出气体的体积和时间的关系如下图所示.请依图回答下列问题:
(1)实验时放出气体的总体积为______;
(2)放出一半气体所需要的时间为______;
(3)ABCD四点化学反应速率的由快到慢顺序为______
(4)解释反应速率的大小变化原因______
;
(5)在5min后,收集到的气体体积不再增加,原因是______.
答案
(1)由反应方程式为:2H2O2
2H2O+O2↑,该反应为不可逆反应,在5min后,收集到的气体体积不再增加,说明过氧化氢完全分解,由图象可知,生成氧气的体积为60mL,故答案为:60ml; MnO2 .
(2)由图象可知,当时间进行到1min时,需要的时间为1min,故答案为:1 min;
(3)反应物浓度大小决定反应速率大小,随着反应的进行,双氧水的浓度逐渐减小,反应速率也随着减小,
故答案为:D>C>B>A;
(4)浓度越大,反应速率越大,反之越小,随着反应进行,反应物的浓度逐渐减小,则速率逐渐减小,
故答案为:随着反应的进行,双氧水的浓度逐渐减小,反应速率也随着减小;
(5)该反应为不可逆反应,在5min后,收集到的气体体积不再增加,说明过氧化氢完全分解,
故答案为:此时双氧水已完全分解.
