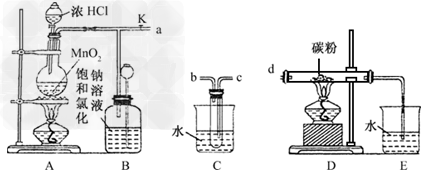
有A、B、C、D四种物质,如图所示,A、B、C在一定下可以发生转化,在C溶液中通入CO2,溶液变浑浊,生成白色沉淀A.D与A、B、C均能发生反应,D与C发生中和反应,D与A反应有CO2气体产生,D与AgNO3溶
液反应,可产生不溶于稀硝酸的白色沉淀.
(1)请根据已知条件推断四种物质的化学式:A______B______C______D______
(2)请写出下列反应的化学方程式:C溶液中通入CO2,溶液变浑浊______D与A反应______.
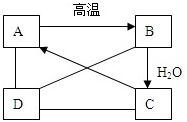
①根据题意“在C溶液中通入CO2,溶液变浑浊,生成白色沉淀A.”可以判断,C为Ca(OH)2,A为CaCO3;反应的化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O;
②由提示A
B可得:CaCO3高温
CaO+CO2,故B为CaO; 高温 .
③根据题意“D与AgNO3溶液反应,可产生不溶于稀硝酸的白色沉淀”可知D为HCl,反应的化学方程式为:AgNO3+HCI=AgCI↓+HNO3;
④D与A反应的化学方程式为:CaCO3+2HCI=CaCl2+H2O+CO2↑.
故答案为:(1)CaCO3,CaO,Ca(OH)2,HCl;
(2)Ca(OH)2+CO2=CaCO3↓+H2O,CaCO3+2HCI=CaCl2+H2O+CO2↑.