问题
填空题
下表是元素周期表的一部分。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | D | F | H | |||||
| 3 | B | C | E | G |
(1)单质中氧化性最强的是_______,还原性最强的是_____,化学性质最不活泼的是______。
(2)最高价氧化物对应水化物的酸性最强的酸是_________,最稳定的氢化物是__________。
(3)按碱性逐渐减弱、酸性逐渐增强的顺序,将B、C、E、G四种元素的最高价氧化物对应水化物的化学式排列成序是__________。
(4)D、E、F三种元素按原子半径由大到小的顺序排列为__________。
(5)A的氧化物常温下呈__________态,它和B的单质反应后所得溶液的pH__________7。
(6)B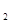 D
D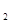 的电子式为________,其中化学键的类型有________ 。
的电子式为________,其中化学键的类型有________ 。
答案
(1)F2 Na Ne(2)HClO4 HF(3)NaOH、Al(OH)3、H3PO4、HClO4
(4)E>D>F(5)液 >(6)  离子键、共价键
离子键、共价键
题目分析:A-H各元素分别为H、Na、Al、N、P、F、Cl、Ne。同周期元素,从左到右,非金属性逐渐增强;同主族元素,从上到下,金属性逐渐增强。
(1)单质中氧化性最强的是F2,还原性最强的是Na;(2)F没有最高价氧化物对应水化物;(4)原子半径大小的判断:①先比较电子层数,电子层数多的半径大②若电子层数相同,再比较核电荷数,核电荷数大的半径大。(5)A的氧化物为H2O,和Na反应后所得溶液为NaOH,强碱。
点评:元素周期表及其规律是高考必考知识点,考生在备考中应注意积累掌握短周期元素的结构与性质。
