(15分)(1)25℃时,0.1 mol·L-1的HA溶液中c(H+)/c(OH-)=1010。请回答下列问题:
①HA是________(填“强电解质”或“弱电解质”);
②在加水稀释HA溶液的过程中,随着水量的增加而减小的是________(填字母)。
A.c(H+)/c(HA) B.c(HA)/(A-) C.c(H+)与c(OH-)的乘积 D.c(OH-)
③若M溶液是由上述HA溶液V1 mL与pH = 12的NaOH溶液V2 mL混合充分反应而得,则下列说法中正确的是
A.若溶液M呈中性,则溶液M中c(H+) + c(OH-) = 2.0×10-7 mol·L-1
B.若V1 =V2 ,则溶液M的pH一定等于7
C.若溶液M呈酸性,V1一定大于V2
D.若溶液M呈碱性,V1一定小于V2
(2)若已知在25℃,AgCl的Ksp = 1.8×10-10,现将足量AgCl分别放入:①100 mL 蒸馏水中;②100 mL 0.2mol·L-1 AgNO3溶液中;③100 mL 0.1mol·L-1 AlCl3溶液中;④100 mL 0.1mol·L-1盐酸中,充分搅拌后,相同温度下c(Ag+)由大到小的顺序是 (用序号连接)
(3)若1mol SO2(g)氧化为1mol SO3(g)的ΔH =-99kJ·mol-1,单质硫的燃烧热为296kJ·mol-1,则由S(s)生成3 mol SO3(g)的ΔH =
(4)对于2NO2(g) N2O4(g) ΔH < 0反应,在温度为T1,T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。则下列说法正确的是 。
N2O4(g) ΔH < 0反应,在温度为T1,T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。则下列说法正确的是 。
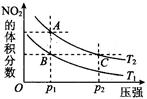
①.A、C两点的反应速率:A>C
②.A、C两点气体的颜色:A深、C浅
③.B、C两点的气体的平均分子质量:B<C
④.由状态B到状态A,可以用加热方法
(5)下图是利用甲烷燃料电池电解50 mL 2 mol·L-1的氯化铜溶液的装置示意图: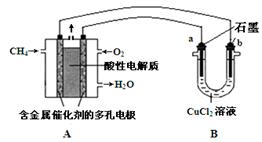
请回答:
① 甲烷燃料电池的负极反应式是 。
② 当线路中有0.2 mol电子通过时,阴极增重____g。
(1)①弱电解质(1分) ②B(2分) ③A D(2分)(2)②>①>④>③(2分)
(3)-1185 kJ·mol-1(2分) (4)④(2分)
(5)CH4 —8e— + 2H2O=CO2 + 8H+(2分) 6.4(2分)
题目分析:(1)①25℃时,0.1 mol·L-1的HA溶液,若HA是强酸,则c(H+)/c(OH-)=1012,实际上则c(H+)/c(OH-)=1010,所以HA是弱酸,是弱电解质;②A.HA是弱酸,加水稀释促进电离,溶液中氢离子的物质的量增大,HA的物质的量减小,相同溶液中:n(H+)/n(HA)=c(H+)/c(HA),其比值增大,错误;B.HA是弱酸,加水稀释促进电离,溶液中A—的物质的量增大,HA的物质的量减小,相同溶液中:n(HA)/n(A-)=c(HA)/c(A-),其比值减小,正确;C.c(H+)与c(OH-)的乘积为水的离子积,温度不变,水的离子积常数不变,错误;D.加水稀释促进酸电离,氢离子浓度降低,但氢氧根离子浓度增大,错误;选B;③A.若溶液M呈中性,则c(H+)=c(OH-)=1×10-7mol•L-1,则c(H+)+c(OH-)=2×10-7mol•L-1,正确;B.若V1=V2,HA远过量,溶液M的pH小于7,错误;C.HA为弱酸,M溶液呈酸性,则V1不一定大于V2,错误;D.HA为弱酸,溶液呈碱性,V1一定小于V2,正确;选:AD;(2)②AgCl分别放入100mL 0.2mol•L-1AgNO3溶液中Ag+浓度为0.2mol/l抑制氯化银沉淀溶解,③AgCl分别放入100mL 0.1mol•L-1氯化铝溶液中氯离子浓度为0.3mol/L,银离子浓度=6×10-10mol/L;④AgCl分别放入100mL 0.1mol•L-1盐酸溶液中氯离子浓度为0.1mol/L,银离子为1.8×10-9mol/L;综上所述大小顺序为:②>①>④>③;(3)单质硫的燃烧热为296kJ•mol-1,则S(s)+O2(g)=SO2(g)△H=-296kJ•mol-1,而 1mol SO2(g)氧化为1mol SO3的△H=-99kJ•mol-1,则SO2(g)+1/2O2(g)=SO3(g)△H=-99kJ•mol-1,由盖斯定律可得:S(s)+3/2O2(g)=SO3(g)△H=-296kJ•mol-1+(-99kJ•mol-1)=-395kJ•mol-1,所以S(s)生成3mol SO3(g)的△H为-395kJ•mol-1×3=-1185 kJ•mol-1;(4)2NO2(g) N2O4(g) ΔH < 0,该反应为放热反应,升高温度,化学平衡逆向移动,NO2的体积分数增大;增大压强,化学平衡正向移动,NO2的体积分数减小。①由图象可知,A、C两点均在温度为T2的等温线上,C的压强大,则A、C两点的反应速率:A<C,错误;②由图象可知,C的压强大,体积小,则C各物质的浓度大,则a、c两点气体的颜色:A浅,C深,错误;③B、C两点的气体的体积分数相等,平均分子质量:B=C,错误;④升高温度,化学平衡逆向移动,NO2的体积分数增大,由图象可知,A点NO2的体积分数大,则T1<T2,由状态B到状态A,可以用加热的方法,正确;选④;(5)①原电池负极发生氧化反应,甲烷在负极通入,酸性条件下,发生氧化反应生成CO2、H+,负极电极反应式为:CH4-8e-+2H2O=CO2+8H+;②B为电解池,铜离子发生还原反应,在阴极析出,转移0.2mol电子,析出铜的物质的量为0.1mol,质量为6.4g。
N2O4(g) ΔH < 0,该反应为放热反应,升高温度,化学平衡逆向移动,NO2的体积分数增大;增大压强,化学平衡正向移动,NO2的体积分数减小。①由图象可知,A、C两点均在温度为T2的等温线上,C的压强大,则A、C两点的反应速率:A<C,错误;②由图象可知,C的压强大,体积小,则C各物质的浓度大,则a、c两点气体的颜色:A浅,C深,错误;③B、C两点的气体的体积分数相等,平均分子质量:B=C,错误;④升高温度,化学平衡逆向移动,NO2的体积分数增大,由图象可知,A点NO2的体积分数大,则T1<T2,由状态B到状态A,可以用加热的方法,正确;选④;(5)①原电池负极发生氧化反应,甲烷在负极通入,酸性条件下,发生氧化反应生成CO2、H+,负极电极反应式为:CH4-8e-+2H2O=CO2+8H+;②B为电解池,铜离子发生还原反应,在阴极析出,转移0.2mol电子,析出铜的物质的量为0.1mol,质量为6.4g。
