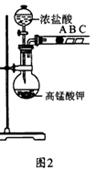
学习了元素周期律的有关知识后,同学们设计了多个实验在实验室探究同周期及同主族元素性质的递变规律。甲组同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成同主族和同周期元素非金属性强弱比较的实验研究;乙组同学设计了如图2装置来验证卤素单质氧化性的相对强弱的实验。
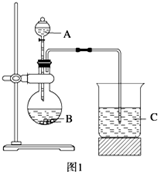
(1) 甲组同学设计实验的依据是 ;写出选用物质的名称:A 、B 、C ;烧杯C中发生反应的离子方程式 ,通过实验得出的结论:元素非金属性强弱顺序为 。
(2) 乙组同学实验过程如下:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为棕色时,关闭活塞a。
Ⅳ………
①验证氯气的氧化性强于碘的实验现象是 。
②B中溶液发生反应的离子方程式是 。
③为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是
。
④过程Ⅲ实验的目的是 。
⑤氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下 , 能力逐渐减弱。
(16分)
(1)(6分) 强酸制弱酸 硝酸 碳酸钙 硅酸钠
CO2+SiO32-+H2O=H2SiO3↓+CO32- N 〉C 〉 Si
(2) (10分)
①淀粉KI试纸变蓝
②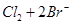

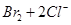
③打开活塞b,将少量C中溶液滴入D中,关闭活塞b,取下D振荡。静止后CCl4层溶液变为紫红色
④确认C的黄色溶液中五Cl2,排除Cl2对溴置换碘实验的干扰
⑤原子半径逐渐增大 得电子能力
题目分析:(1)验证元素非金属性与对应最高价含氧酸之间的关系,所选取的酸应为稀硝酸,圆底烧瓶内的固体药品应为大理石,不能用碳酸钠粉末,反应剧烈,不易控制反应,C中应盛装硅酸钠溶液,以此来证明硝酸、碳酸以及硅酸的酸性强弱。C中盛装硅酸钠溶液,由于碳酸酸性比硅酸强,在C中通入二氧化碳气体生成硅酸沉淀,反应的离子方程式为CO2+SiO32-+H2O=H2SiO3↓+CO32-。
(2)单质的氧化性Cl2>Br2>I2,则
①氯气和KI溶液反应生成单质碘,淀粉变蓝,故答案为:试纸变蓝。
②氯气通入溴化钠溶液中发生置换反应生成溴,反应的离子方程式为Cl2+2Br-=Br2+2Cl-,
故答案为:Cl2+2Br-=Br2+2Cl-。
③验证溴的氧化性强于碘,过程Ⅳ的操作和现象是打开活塞b,将少量C中溶液滴入D中,关闭活塞b,取下D振荡。静止后CCl4层溶液变为紫红色。
④根据题中信息分析得知,过程Ⅲ实验的目的是确认C的黄色溶液中五Cl2,排除Cl2对溴置换碘实验的干扰。
⑤根据以上分析得,氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下原子半径逐渐增大,得电子能力能力逐渐减弱。
点评:本题考查非金属性强弱比较的实验设计,题目难度不大,注意实验设计的原理和方法。
